Thuộc tính Natri Hydride (NaH), Khả năng phản ứng, Nguy cơ và Công dụng
các natri hydrua là một hợp chất vô cơ có công thức NaH. Nó có một liên kết ion giữa natri và hydride. Cấu trúc của nó được minh họa trong hình 1. Nó là đại diện của hydrua muối, có nghĩa là nó là một hydrua tương tự như muối, bao gồm các ion Na + và H-, trái ngược với các hydrua phân tử hơn như borane, metan, amoniac và nước.
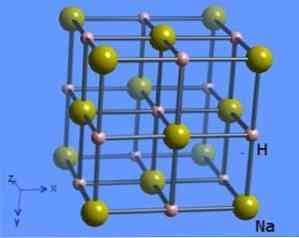
Cấu trúc tinh thể có tọa độ số 6, trong đó mỗi phân tử natri được bao quanh bởi 8 ion hydride có hình bát diện và được minh họa trong hình 2 (Mark Winter [Đại học Sheffield và WebElements Ltd, 1993-2016).
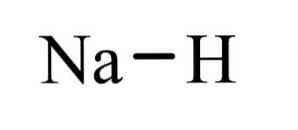
Hợp chất được điều chế bằng phản ứng trực tiếp giữa natri và khí hydro (Công thức natri hydrua - Công dụng, tính chất, cấu trúc và công thức của natri hydrua, 2005-2017) như sau:
H2 + 2Na → 2NaH
Natri hydride được bán thương mại dưới dạng phân tán 60% w / w (tỷ lệ phần trăm theo trọng lượng) trong dầu khoáng để xử lý an toàn (SODIUM HYDRIDE, s.f.).
Chỉ số
- 1 Tính chất lý hóa của natri hydrua
- 2 Tính phản ứng và mối nguy hiểm
- 3 công dụng
- 4 tài liệu tham khảo
Tính chất lý hóa của natri hydrua
Natri hydride là chất rắn màu trắng khi nó nguyên chất mặc dù nó thường thu được bằng màu xám hoặc bạc. Sự xuất hiện của nó được thể hiện trong hình 3.

NaH có trọng lượng phân tử 23,99771 g / mol, mật độ 1,394 g / ml và nhiệt độ nóng chảy 800 ° C (Hiệp hội hóa học Hoàng gia, 2015). Nó không hòa tan trong amoniac, benzen, carbon tetraclorua và carbon disulfide (Trung tâm thông tin công nghệ sinh học quốc gia, s.f.).
Các hợp chất là cực kỳ không ổn định. NaH tinh khiết có thể dễ dàng bốc cháy trong không khí. Khi tiếp xúc với nước có trong không khí, nó sẽ giải phóng hydro rất dễ cháy.
Khi mở ra không khí và hơi ẩm, NaH cũng dễ dàng bị thủy phân thành bazơ natri hydroxit (NaOH) ăn mòn mạnh theo phản ứng:
NaH + H2O → NaOH + H2
Trong phản ứng này có thể thấy rằng natri hydride hoạt động giống như một bazơ. Điều này là do độ âm điện.
Natri có độ âm điện thấp hơn đáng kể (≈1,0) so với hydro (≈2,1), có nghĩa là hydro chiết xuất mật độ electron về phía chính nó, di chuyển ra khỏi natri để tạo ra cation natri và anion của hydrua.
Để một hợp chất là axit Brønsted, nó cần tách mật độ electron khỏi hydro, nghĩa là kết nối nó với một nguyên tử có độ âm điện như oxy, flo, nitơ, v.v. Chỉ sau đó, nó mới có thể được mô tả chính thức là H + và nó có thể được phân tách như vậy không.
Một hydrua được mô tả tốt hơn nhiều là H- và có một cặp electron tự do. Như vậy, nó là một bazơ Brønsted, không phải là axit. Trên thực tế, nếu bạn mở rộng định nghĩa axit / bazơ Brønsted theo cách mà Lewis đã làm, bạn sẽ đi đến kết luận rằng natri (Na +) là loài axit ở đây.
Sản phẩm phản ứng axit / bazơ Brønsted của bazơ H- và axit H + trở thành H2. Do hydro axit được chiết xuất trực tiếp từ nước, khí hydro có thể sủi bọt, thay thế trạng thái cân bằng ngay cả khi phản ứng không được ưa chuộng về mặt nhiệt động.
Các ion OH- có thể được viết lại với phần còn lại của cation Na + để cung cấp natri hydroxit (Tại sao natri hydrua rắn lại không phải là axit khi phản ứng với nước ?, 2016).
Tính phản ứng và mối nguy hiểm
Các hợp chất là một chất khử mạnh mẽ. Tấn công SiO2 trong thủy tinh. Nó bốc cháy khi tiếp xúc với khí F2, Cl2, Br2 và I2 (sau này ở nhiệt độ trên 100 ° C), đặc biệt là khi có hơi ẩm, tạo thành HF, HCl, HBr và HI.
Phản ứng với lưu huỳnh để cho Na2S và H2S. Nó có thể phản ứng bùng nổ với dimethyl sulfoxide. Phản ứng mạnh mẽ với acetylene, thậm chí ở -60 ° C. Nó dễ cháy tự nhiên trong flo.
Nó bắt đầu phản ứng trùng hợp trong ethyl-2,2,3-trifluoropropionate, do đó este bị phân hủy mạnh. Sự hiện diện trong phản ứng của diethyl succinate và ethyl trifluoroacetate, đã gây ra vụ nổ (SODIUM HYDRIDE, 2016).
Natri hydride được coi là ăn mòn cho da hoặc mắt, do tiềm năng của sản phẩm phụ ăn da của các phản ứng với nước.
Trong trường hợp tiếp xúc với mắt, chúng cần được rửa sạch với một lượng nước lớn, dưới mí mắt trong ít nhất 15 phút và tìm kiếm sự chăm sóc y tế ngay lập tức..
Trong trường hợp tiếp xúc với da, chải ngay lập tức và rửa sạch vùng bị ảnh hưởng bằng nước. Tìm kiếm sự chăm sóc y tế nếu kích thích vẫn còn.
Nó có hại do ăn phải do phản ứng với nước. Không gây nôn. Bạn nên đi khám ngay lập tức và chuyển nạn nhân đến trung tâm y tế.
Sự phân tán natri hydride trong dầu không phải là bụi. Tuy nhiên, vật liệu phản ứng có thể phát ra sương mù ăn da mịn. Trong trường hợp hít phải, súc miệng bằng nước và chuyển nạn nhân đến nơi có không khí trong lành. Cần được chăm sóc y tế (Rhom và Hass Inc., 2007).
Công dụng
Công dụng chính của natri hydride là thực hiện các phản ứng ngưng tụ và kiềm hóa phát triển thông qua sự hình thành của một carbanion (được xúc tác bởi bazơ).
Natri hydrua trong dầu tương tự như natri và natri kim loại, trong khả năng hoạt động như một chất khử liên kết trong este acetoacetic, Claisen, Stobbe, Dieckmann và các phản ứng liên quan khác. Nó đã đánh dấu những lợi thế so với các chất ngưng tụ khác ở chỗ:
- Nó là một cơ sở mạnh mẽ hơn, dẫn đến sự mất liên kết trực tiếp hơn.
- Không cần thừa.
- H2 được tạo ra cho phép đo mức độ phản ứng.
- Phản ứng thứ cấp như giảm được loại bỏ.
Các phản ứng kiềm hóa các amin thơm và dị vòng như 2-aminopyridine và phenothiazine có thể dễ dàng đạt được ở năng suất cao khi sử dụng hỗn hợp toluene-methylformamide. Nồng độ của dimethylformamide là một biến được sử dụng để kiểm soát tốc độ phản ứng (HINCKLEY, 1957).
Việc sử dụng natri hydrua để lưu trữ hydro để sử dụng trong các phương tiện pin nhiên liệu đã được đề xuất, hydrua được bọc trong các hạt nhựa được nghiền nát trong sự hiện diện của nước để giải phóng hydro.
Tài liệu tham khảo
- HINCKLEY, M. D. (1957). Sản xuất, xử lý và sử dụng Natri hydride. Những tiến bộ trong hóa học, tập 19, 106-117.
- Mark Winter [Đại học Sheffield và WebElements Ltd, Hoa Kỳ (1993-2016). Natri: natri hydrua. Lấy từ WebElements: webelements.com.
- Trung tâm Thông tin Công nghệ sinh học Quốc gia. (s.f.). Cơ sở dữ liệu hợp chất PubChem; CID = 24758. Lấy từ PubChem: pubool.ncbi.nlm.nih.gov.
- Rhom và Hass inc. (2007, tháng 12). Natri hydride 60% phân tán trong dầu. Lấy từ dow.com.
- Hội hóa học hoàng gia. (2015). Natri hydrua. Lấy từ ChemSpider: chemspider.com.
- SODIUM HYDRIDE. (2016). Lấy từ các hóa chất: cameochemicals.noaa.gov.
- Công thức natri hydride - Công dụng, tính chất, cấu trúc và công thức của natri hydrua. (2005-2017). Lấy từ Softschools.com: softschools.com.
- SODIUM HYDRIDE. (s.f.). Lấy từ chemicalland21: chemicalland21.com.
- Tại sao natri hydride rắn dựa trên và không axit khi phản ứng với nước? (2016, ngày 20 tháng 4). Lấy từ stackexchange: chem.stackexchange.com.


