Phản ứng xà phòng hóa và các chất có thể thu được
các xà phòng hóa Đây là sự thủy phân cơ bản của một este. Điều này có nghĩa là este phản ứng với một bazơ (NaOH hoặc KOH) không thể đảo ngược, tạo ra rượu và carboxylat natri hoặc kali. Từ này có nghĩa là "sản xuất xà phòng" và trên thực tế, là một trong những phản ứng hóa học lâu đời nhất được nhân loại sử dụng.
Vào thời Babylon, với sự trợ giúp của tro được thu thập từ gỗ và thực vật và mỡ động vật, họ đã hoàn thiện nghệ thuật làm xà phòng. Vì sao động vật béo? Lý do là nó rất giàu chất tri glycerol (triglyceride) và tro gỗ là nguồn cung cấp kali, kim loại cơ bản.
Mặt khác, phản ứng tiến tới năng suất thấp hơn, nhưng đủ để phản ánh tác động của nó lên sơn và một số bề mặt. Đó là trường hợp của tranh sơn dầu, trong đó các sắc tố được trộn với dầu (nguồn este).
Chỉ số
- 1 phản ứng xà phòng hóa
- 1.1 Cơ chế
- 1.2 Động học
- 2 chất có thể thu được bằng cách xà phòng hóa
- 2.1 Hành động dung môi của xà phòng
- 3 tài liệu tham khảo
Phản ứng xà phòng hóa
Cơ chế
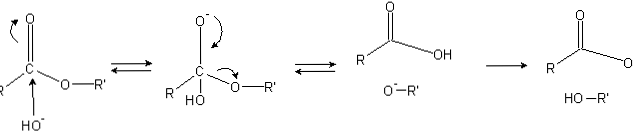
Các este có nhóm acyl (O = C-R), dễ bị tấn công nucleophilic như OH-.
Do các nguyên tử oxy "đánh cắp" mật độ điện tử từ nguyên tử carbon, nên nó được tích điện một phần, thậm chí còn nhiều hơn trong trường hợp este.
Do đó, điện tích dương này thu hút các loài âm có khả năng cung cấp điện tử cho nguyên tử carbon, với sự tấn công nucleophin xảy ra (phía bên trái của hình ảnh). Kết quả là một trung gian tứ diện (phân tử thứ hai từ trái sang phải) được hình thành.
Điện tích âm trên oxy của chất trung gian tứ diện là tích của OH- xung quanh Sau đó, điện tích âm này được hủy bỏ để tạo ra nhóm carbonyl, "buộc" sau đó phá vỡ liên kết C-OR '. Ngoài ra, sự di chuyển này tạo ra RCOOH axit carboxylic và ion kiềm R'O-.
Cuối cùng, vì môi trường phản ứng là cơ bản, nên kiềm hóa khử một phân tử nước và axit cacboxylic phản ứng với một OH khác- của môi trường, tạo ra các sản phẩm xà phòng hóa.
Động học
Tốc độ của phản ứng xà phòng hóa tỷ lệ thuận với nồng độ của các chất phản ứng. Nói cách khác, tăng nồng độ của este (RCOOR ') hoặc bazơ (NaOH), phản ứng sẽ diễn ra với tốc độ cao hơn.
Điều này cũng được dịch như sau: tốc độ xà phòng hóa là thứ tự đầu tiên đối với este và thứ tự đầu tiên đối với cơ sở. Trên đây có thể được biểu thị với phương trình toán học sau:
Tốc độ = k [RCOOR '] [NaOH]
Trong đó k là hệ số không đổi hoặc tốc độ, thay đổi theo hàm của nhiệt độ hoặc áp suất; nghĩa là, nhiệt càng cao thì tốc độ xà phòng hóa càng lớn. Vì lý do này, phương tiện có thể sôi.
Vì cả hai thuốc thử đều có động năng bậc 1, nên phản ứng tổng thể là bậc hai.
Trong cơ chế phản ứng xà phòng hóa, sự hình thành trung gian tứ diện đòi hỏi sự tấn công nucleophin, bao gồm cả este và bazơ.
Do đó, động học bậc hai được phản ánh trong thực tế này, bởi vì chúng can thiệp vào bước xác định (chậm) của phản ứng.
Những chất có thể thu được bằng cách xà phòng hóa

Các sản phẩm chính của quá trình xà phòng hóa là rượu và muối của axit cacboxylic. Trong môi trường axit, RCOOH tương ứng, thu được từ quá trình xà phòng hóa chất béo và dầu, được gọi là axit béo, thu được..
Theo cách này, xà phòng bao gồm muối của các axit béo do xà phòng hóa. Bạn có đi ra ngoài với những cation? Họ có thể là Na+, K+, Mg2+, Đức tin3+, v.v..
Các muối này hòa tan trong nước, nhưng kết tủa bởi tác dụng của NaCl được thêm vào hỗn hợp, làm mất nước xà phòng và tách nó ra khỏi pha nước. Phản ứng xà phòng hóa cho một chất béo trung tính như sau:
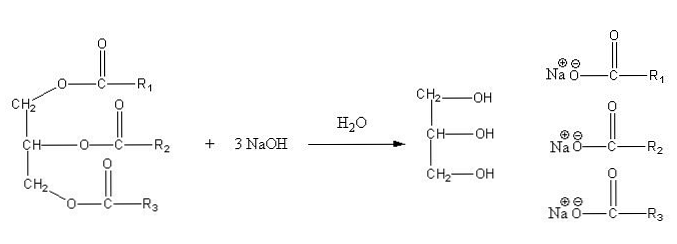
Glycerin là "E" có cồn và xà phòng là tất cả các muối của axit béo thu được. Ở đây, mỗi sidechain -R có độ dài và mức độ không bão hòa khác nhau. Do đó, các chuỗi này tạo ra sự khác biệt giữa chất béo và dầu thực vật.
Chìa khóa để sản xuất xà phòng sau đó nằm ở việc lựa chọn các chất béo và dầu tốt nhất, hay cụ thể hơn là trong việc lựa chọn các nguồn chất béo trung tính khác nhau.
Khối xà phòng trắng này có thể chứa thuốc nhuộm và các hợp chất hữu cơ khác trong cấu trúc của nó, mang lại cho nó mùi thơm dễ chịu và màu sắc tươi sáng. Từ đây, một loạt các khả năng được thuần hóa bởi nghệ thuật và ơn gọi trong thương mại này.
Tuy nhiên, phản ứng xà phòng hóa cũng là một con đường tổng hợp của axit cacboxylic và rượu không nhất thiết phải làm với glycerin hoặc xà phòng.
Ví dụ, thủy phân cơ bản của bất kỳ este nào, chẳng hạn như ethyl acetate đơn giản, sẽ tạo ra axit axetic và ethanol.
Hành động dung môi của xà phòng

Các muối của axit béo hòa tan trong nước, nhưng không giống như các ion được hòa tan; đó là, được bao quanh bởi một quả cầu nước. Trong trường hợp xà phòng, chuỗi bên của chúng -R ngăn chúng theo lý thuyết hòa tan trong nước.
Do đó, để chống lại vị trí không thoải mái về mặt năng lượng này, chúng được định hướng theo cách mà các chuỗi này tiếp xúc với nhau, tạo thành một hạt nhân hữu cơ cực, trong khi các đầu cực, đầu cuối (-COO)- Na+), tương tác với các phân tử nước và tạo ra một "vỏ cực".
Trên đây được minh họa trong hình trên, trong đó loại cấu trúc được gọi là micelle được hiển thị.
"Đuôi đen" tương ứng với các chuỗi kỵ nước, bị vướng vào lõi hữu cơ được bảo vệ bởi các quả cầu màu xám. Những quả cầu màu xám này tạo thành lá chắn cực, các đầu -COO- Na+.
Sau đó, các mixen là các cụm (cụm) muối của các axit béo. Trong đó, chúng có thể chứa chất béo, không hòa tan trong nước vì đặc tính phân cực của nó.
Làm thế nào để họ làm điều đó? Cả hai chuỗi chất béo và -R đều kỵ nước, vì vậy cả hai đều có ái lực lớn với nhau.
Khi các mixen bao bọc các chất béo, nước tương tác với vỏ cực, cho phép khả năng hòa tan của xà phòng. Tương tự như vậy, các mixen được tích điện âm, gây ra lực đẩy lẫn nhau và do đó, tạo ra sự phân tán của chất béo.
Tài liệu tham khảo
- Anne Marie Helmenstine, tiến sĩ (Ngày 3 tháng 10 năm 2017). Định nghĩa và phản ứng xà phòng hóa. Truy cập ngày 24 tháng 4 năm 2018, từ: thinkco.com
- Đức Phanxicô A. Carey. Hóa hữu cơ Axit cacboxylic. (ấn bản thứ sáu., trang 863-866). Đồi Mc Graw.
- Graham Solomons T.W., Craig B. Fryhle. Hóa hữu cơ. Lipid (tái bản lần thứ 10., Trang 1056-1058). Wiley Plus.
- Wikipedia. (2018). Xà phòng hóa. Truy cập ngày 24 tháng 4 năm 2018, từ: en.wikipedia.org
- Boyd C. (ngày 27 tháng 2 năm 2015). Hiểu hóa học và lịch sử của xà phòng. Truy cập ngày 24 tháng 4 năm 2018, từ: chemservice.com
- Luca Laghi (27 tháng 3 năm 2007). Xà phòng hóa. Truy cập ngày 24 tháng 4 năm 2018, từ: commons.wikidia.org
- Móc Amanda (Ngày 12 tháng 5 năm 2015). Micelle (thang độ xám). Truy cập ngày 24 tháng 4 năm 2018, từ: commons.wikidia.org


