Ammonium Sulfate Cấu trúc, tính chất và công dụng
các amoni sunfat Nó là một muối vô cơ ternary và ammoniacal của axit sulfuric. Công thức hóa học của nó là (NH4)2VẬY4. Do đó, tỷ lệ cân bằng hóa học nói rằng đối với mỗi anion sunfat có hai cation amoni tương tác với nó. Điều này cho phép tính trung lập của muối ((+1) 2 + (-2)).
Danh pháp của nó là do thực tế rằng nó là một loại muối có nguồn gốc từ H2VẬY4, thay đổi hậu tố "uric" thành "ato". Do đó, hai proton ban đầu được thay thế bằng NH4+, sản phẩm phản ứng với amoniac (NH3). Khi đó, phương trình hóa học để tổng hợp của nó là: 2 NH3 + H2VẬY4 => (NH4)2VẬY4
Ammonium sulfate là một cửa hàng nitơ và lưu huỳnh, cả hai không thể thiếu trong hóa học của đất và phân bón.
Chỉ số
- 1 Cấu trúc hóa học
- 2 Tính chất lý hóa
- 2.1 Trọng lượng phân tử
- 2.2 Ngoại hình
- 2.3 Mùi
- 2.4 Điểm nóng chảy
- 2.5 Độ hòa tan
- Mật độ 2,6
- 2.7 Áp suất hơi
- 2.8 Điểm chớp cháy
- 2,9 pH
- 2.10 Ổn định
- 2.11 Phân hủy
- 2.12 Ăn mòn
- 3 công dụng
- 3.1 Trong nông nghiệp
- 3.2 Là thuốc thử phân tích
- 3.3 Trong sự kết tủa và phân lập protein
- 3,4 trong ngành
- 3.5 Công dụng khác
- 4 tài liệu tham khảo
Cấu trúc hóa học
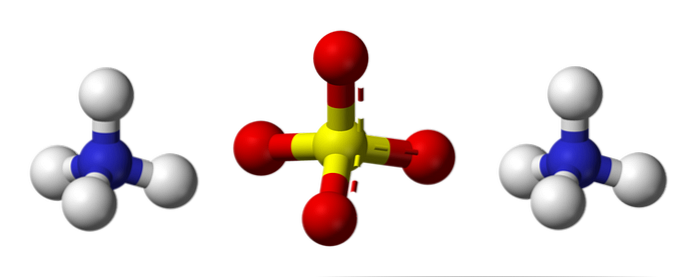
Hình trên minh họa hình học phân tử của các ion NH4+ và SO42-. Các quả cầu đỏ tương ứng với các nguyên tử oxy, các quả cầu trắng tương ứng với các nguyên tử hydro, các quả cầu xanh với nguyên tử nitơ và các quả cầu vàng tương ứng với nguyên tử lưu huỳnh.
Cả hai ion có thể được coi là hai khối tứ diện, do đó có ba đơn vị tương tác để tạo thành một sắp xếp tinh thể trực giao. Anion sunfat là SO42- và có thể quyên góp hoặc chấp nhận bốn liên kết hydro, giống như cation NH4+.
Tính chất hóa lý
Trọng lượng phân tử
132.134 g / mol.
Ngoại hình
Màu trắng đặc. Tinh thể trắng hoặc nâu trực tràng, tùy thuộc vào mức độ tạp chất.
Mùi
Nhà vệ sinh.
Điểm nóng chảy
280 ºC. Điểm nóng chảy này, thấp so với các hợp chất ion khác, là do nó là một loại muối có các cation đơn trị (+1) và với các ion không giống nhau về kích thước của nó, làm cho chất rắn có năng lượng hình tinh thể thấp.
Độ hòa tan
76,4 g / 100 g nước ở 25 ºC. Ái lực này đối với nước là do khả năng lớn của các phân tử của nó để hòa tan các ion amoni. Mặt khác, nó không hòa tan trong acetone và trong rượu; đó là, trong dung môi ít cực hơn nước.
Mật độ
1,77 g / cm3 ở 25 ºC.
Áp suất hơi
1.871 kPa ở 20 ºC.
Điểm dễ cháy
26 ºC.
pH
5.0-6.0 (25 ° C, dung dịch 1 M). Độ pH hơi axit là do thủy phân NH4+ trong nước, sinh ra H3Ôi+ ở nồng độ thấp.
Ổn định
Ổn định trong điều kiện môi trường phù hợp. Tiếp xúc với chất oxy hóa mạnh có thể bắt lửa.
Phân hủy
Nó bắt đầu phân hủy ở 150 ºC, giải phóng hơi độc của oxit lưu huỳnh, oxit nitơ và amoni.
Ăn mòn
Không tấn công sắt hoặc nhôm.
Công dụng

Trong nông nghiệp
- Ammonium sulfate được sử dụng làm phân bón trong đất kiềm. Muối amoni có 21% nitơ và 24% lưu huỳnh trong thành phần của nó. Tuy nhiên, có những hợp chất cung cấp một lượng nitơ lớn hơn ammonium sulfate; Ưu điểm của loại thứ hai là nồng độ lưu huỳnh cao.
- Lưu huỳnh rất cần thiết trong quá trình tổng hợp protein, vì một số axit amin - như cystine, methionine và cysteine - có lưu huỳnh. Vì những lý do này, ammonium sulfate tiếp tục là một trong những loại phân bón quan trọng nhất.
- Nó được sử dụng trong các vụ mùa lúa mì, ngô, gạo, bông, khoai tây, cây gai dầu và cây ăn quả.
- Độ pH thấp của đất kiềm do đóng góp của chúng vào quá trình nitrat hóa được thực hiện bởi vi khuẩn. Amoni (NH) được sử dụng4+) để sản xuất nitrat (NO3-) và giải phóng H+: 2NH4+ + 4O2 => 2NO3- + 2 giờ2O + 4H+. Sự gia tăng nồng độ hydro làm giảm độ pH của đất kiềm và cho phép sử dụng nhiều hơn.
- Ngoài việc sử dụng làm phân bón, ammonium sulfate hoạt động như một chất đồng hóa cho thuốc trừ sâu hòa tan, thuốc diệt cỏ và thuốc diệt nấm, được phun lên cây trồng..
- Sulfate có khả năng cô lập các ion có trong đất và trong nước tưới cần thiết cho sự sống của một số mầm bệnh nhất định. Trong số các ion mà ammonium sulfate thu được là Ca2+, các Mg2+, đức tin2+ và đức tin3+. Hành động này giúp tăng cường hiệu quả diệt vi khuẩn của các tác nhân được đề cập.
Là thuốc thử phân tích
Ammonium sulfate hoạt động như một chất kết tủa trong phân tích điện hóa, trong môi trường nuôi cấy vi sinh và trong điều chế muối amoni.
Trong sự kết tủa và phân lập protein
Ammonium sulfate được sử dụng trong việc phân lập và tinh chế protein, đặc biệt là protein huyết tương. Một lượng ammonium sulfate được thêm vào huyết tương đến một nồng độ nhất định; do đó, sự kết tủa của một nhóm các protein được gây ra.
Kết tủa được thu thập bằng cách ly tâm và một lượng bổ sung amoni sulfat được thêm vào phần nổi phía trên và, ở một nồng độ mới, sự kết tủa của một nhóm protein khác xảy ra..
Sự lặp lại của quá trình trước đó ở dạng tuần tự cho phép thu được các phân đoạn khác nhau của protein huyết tương.
Trước khi xuất hiện các công nghệ mới của sinh học phân tử, quy trình này cho phép phân lập protein huyết tương có tầm quan trọng lớn trong y học, ví dụ: globulin miễn dịch, các yếu tố đông máu, v.v..
Trong công nghiệp
Ammonium sulfate có tác dụng làm chậm sự bắt đầu của đám cháy trong ngành dệt may. Nó được sử dụng như một chất phụ gia trong ngành công nghiệp mạ điện. Nó cũng được sử dụng trong sản xuất hydro peroxide, amoni clorua, v.v..
Công dụng khác
- Ammonium sulfate được sử dụng như một chất điều chỉnh áp suất thẩm thấu và như một tác nhân kết tủa muối.
- Ở dạng ammonium lauryl sulfate, sức căng bề mặt của nước giảm, do đó cho phép phân tách các chất ô nhiễm bằng cách tăng độ cứng của nước.
- Nó là một chất chống ăn mòn.
- Nó được sử dụng như một chất phụ gia thực phẩm điều chỉnh độ axit trong bột và bánh mì.
Tài liệu tham khảo
- TRẺ EM OECD. (Tháng 10 năm 2004). Amoni sunfat. [PDF] Truy cập ngày 27 tháng 4 năm 2018, từ: inchem.org
- Công ty khảm. (2018). Amoni sunfat. Truy cập ngày 27 tháng 4 năm 2018, từ: cropnutnut.com
- Wikipedia. (2018). Amoni sunfat. Truy cập ngày 27 tháng 4 năm 2018, từ: en.wikipedia.org
- Pubool. (2018). Amoni sunfat. Truy cập ngày 27 tháng 4 năm 2018, từ: pubool.ncbi.nlm.nih.gov UpSticksNGo crew.
- (Ngày 23 tháng 7 năm 2015). [Hình] Truy cập ngày 27 tháng 4 năm 2018, từ: flickr.com
- Paula Papp (Ngày 22 tháng 2 năm 2017). Ammonium sulfate ứng dụng và sử dụng. Truy cập ngày 27 tháng 4 năm 2018, từ: business.com


