Khối lượng nguyên tử Làm thế nào nó khác nhau trong bảng tuần hoàn và ví dụ
các khối lượng nguyên tử là một giá trị tương đối chỉ ra mối quan hệ giữa khối lượng mol của một nguyên tố và mật độ của nó. Vì vậy, khối lượng này phụ thuộc vào mật độ của nguyên tố và mật độ phụ thuộc lần lượt vào pha và cách các nguyên tử được sắp xếp trong phạm vi này.
Vì vậy, thể tích nguyên tử của một nguyên tố Z không giống nhau trong một pha khác với pha thể hiện ở nhiệt độ phòng (lỏng, rắn hoặc khí) hoặc khi nó là một phần của các hợp chất nhất định. Do đó, thể tích nguyên tử của Z trong hợp chất ZA khác với thể tích của Z trong hợp chất ZB.

Tại sao? Để hiểu nó, cần phải so sánh các nguyên tử với, ví dụ, viên bi. Các viên bi, giống như những viên bi của hình ảnh vượt trội, đã xác định rất rõ đường viền vật chất của chúng, được quan sát nhờ bề mặt rực rỡ của nó. Ngược lại, ranh giới của các nguyên tử là khuếch tán, mặc dù chúng có thể được coi là hình cầu từ xa.
Do đó, điều quyết định một điểm nằm ngoài ranh giới nguyên tử là xác suất không tìm thấy electron và điểm này có thể ở xa hoặc gần hạt nhân hơn tùy thuộc vào số lượng nguyên tử lân cận tương tác xung quanh nguyên tử..
Chỉ số
- 1 Khối lượng và bán kính nguyên tử
- 2 công thức bổ sung
- 3 Khối lượng nguyên tử thay đổi như thế nào trong bảng tuần hoàn?
- 3.1 Khối lượng nguyên tử của kim loại chuyển tiếp
- 4 ví dụ
- 4.1 Ví dụ 1
- 4.2 Ví dụ 2
- 5 tài liệu tham khảo
Khối lượng và bán kính nguyên tử
Bằng cách tương tác hai nguyên tử H trong phân tử H2, vị trí của hạt nhân của chúng được xác định cũng như khoảng cách giữa chúng (khoảng cách hạt nhân). Nếu cả hai nguyên tử đều có hình cầu, bán kính là khoảng cách giữa hạt nhân và ranh giới khuếch tán:
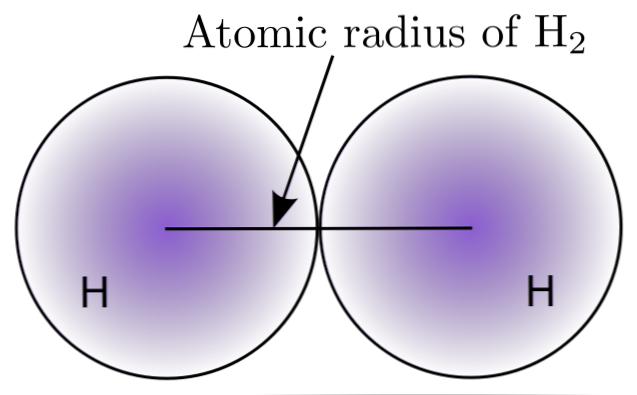
Trong hình trên, có thể thấy xác suất tìm thấy electron giảm khi nó di chuyển ra khỏi hạt nhân. Chia khoảng cách hạt nhân giữa hai, bán kính nguyên tử thu được. Tiếp theo, giả sử hình học hình cầu cho các nguyên tử, chúng tôi sử dụng công thức để tính thể tích của một hình cầu:
V = (4/3) (Pi) r3
Trong biểu thức này r là bán kính nguyên tử được xác định cho phân tử H2. Giá trị của V được tính theo phương pháp không chính xác này có thể thay đổi nếu, ví dụ, nó được coi là H2 ở trạng thái lỏng hoặc kim loại. Tuy nhiên, phương pháp này rất không chính xác vì hình dạng của các nguyên tử nằm cách xa quả cầu lý tưởng trong các tương tác của chúng.
Để xác định khối lượng nguyên tử trong chất rắn, nhiều biến liên quan đến sự sắp xếp được tính đến và chúng được lấy bằng các nghiên cứu nhiễu xạ tia X..
Công thức bổ sung
Khối lượng mol biểu thị lượng vật chất có một mol nguyên tử của nguyên tố hóa học.
Đơn vị của nó là g / mol. Mặt khác, mật độ là khối lượng chiếm một gram của nguyên tố: g / mL. Vì đơn vị của thể tích nguyên tử là mL / mol, bạn phải chơi với các biến để đạt được đơn vị mong muốn:
(g / mol) (mL / g) = mL / mol
Hoặc những gì giống nhau:
(Khối lượng mol) (1 / D) = V
(Khối lượng mol / D) = V
Do đó, có thể dễ dàng tính được thể tích của một mol nguyên tử của một nguyên tố; trong khi với công thức của thể tích hình cầu, thể tích của một nguyên tử riêng lẻ được tính toán. Để đạt được giá trị này từ lần đầu tiên, một chuyển đổi là cần thiết thông qua số của Avogadro (6.02 · 10).-23).
Khối lượng nguyên tử thay đổi như thế nào trong bảng tuần hoàn?
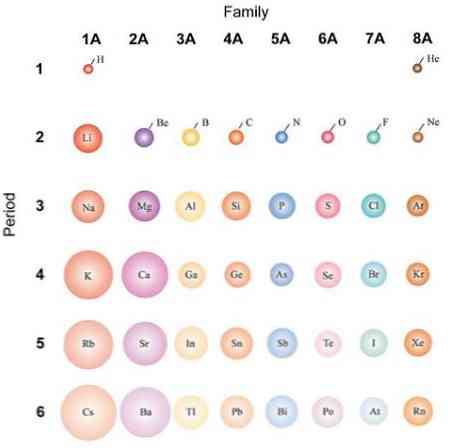
Nếu các nguyên tử được coi là hình cầu, thì sự biến đổi của chúng sẽ giống như được quan sát trong bán kính nguyên tử. Trong hình trên, cho thấy các yếu tố đại diện, nó được minh họa rằng từ phải sang trái các nguyên tử lùn; thay vào đó, từ trên xuống dưới những thứ này trở nên đồ sộ hơn.
Điều này là do trong cùng thời gian, hạt nhân kết hợp các proton khi nó di chuyển sang phải. Những proton này tác dụng một lực hấp dẫn lên các electron bên ngoài, tạo ra điện tích hạt nhân Z hiệu quảef, ít hơn điện tích hạt nhân Z thực tế.
Các electron của các lớp bên trong đẩy lùi các lớp bên ngoài, làm giảm tác dụng của hạt nhân lên các lớp này; Điều này được gọi là hiệu ứng màn hình. Trong cùng thời gian, hiệu ứng màn hình không thể chống lại sự gia tăng số lượng proton, vì vậy các electron ở lớp bên trong không ngăn được sự co lại của các nguyên tử.
Tuy nhiên, bằng cách hạ xuống thành một nhóm, các mức năng lượng mới được kích hoạt, cho phép các electron quay quanh hạt nhân xa hơn. Ngoài ra, số lượng electron ở lớp bên trong tăng lên, có hiệu ứng che chắn bắt đầu bị giảm nếu hạt nhân thêm proton lần nữa.
Vì những lý do này, có thể thấy rằng nhóm 1A có các nguyên tử mạnh nhất, không giống như các nguyên tử nhỏ của nhóm 8A (hoặc 18), là các loại khí hiếm.
Khối lượng nguyên tử của kim loại chuyển tiếp
Các nguyên tử của các kim loại chuyển tiếp kết hợp các electron với quỹ đạo bên trong d. Sự gia tăng hiệu ứng màn hình này và, cũng như điện tích hạt nhân Z thực sự, bị hủy gần như bằng nhau, do đó các nguyên tử của chúng giữ nguyên kích thước tương tự trong cùng thời kỳ.
Nói cách khác: trong một thời kỳ, các kim loại chuyển tiếp thể hiện khối lượng nguyên tử tương tự. Tuy nhiên, những khác biệt nhỏ này rất có ý nghĩa khi xác định các tinh thể kim loại (như thể chúng là viên bi kim loại).
Ví dụ
Hai công thức toán học có sẵn để tính thể tích nguyên tử của một nguyên tố, mỗi công thức có các ví dụ tương ứng.
Ví dụ 1
Cho bán kính nguyên tử của hydro -37 chiều (1 picometer = 10-12m) - và Caesium -265 pm-, tính toán khối lượng nguyên tử của nó.
Sử dụng công thức của thể tích hình cầu, sau đó chúng ta có:
VH= (4/3) (3.14) (37 giờ chiều)3= 212,07 chiều3
VCs= (4/3) (3.14) (265 chiều)3= 77912297,67 chiều3
Tuy nhiên, các thể tích được biểu thị bằng pyromet là cắt cổ, vì vậy chúng được chuyển thành các đơn vị angstroms, nhân chúng với hệ số chuyển đổi (1Å / 100pm)3:
(212,07 chiều3) (1Å / 100pm)3= 2.1207 × 10-4 Å3
(77912297,67 chiều3) (1Å / 100pm)3= 77.9123
Do đó, sự khác biệt về kích thước giữa nguyên tử nhỏ của H và nguyên tử cồng kềnh của Cs vẫn còn rõ ràng về mặt số lượng. Cần phải lưu ý rằng những tính toán này chỉ là gần đúng theo tuyên bố rằng một nguyên tử hoàn toàn hình cầu, đi lang thang khi đối mặt với thực tế.
Ví dụ 2

Mật độ của vàng nguyên chất là 19,32 g / mL và khối lượng mol của nó là 196,97 g / mol. Áp dụng công thức M / D để tính thể tích của một mol nguyên tử vàng có các cách sau:
VÂu= (196,97 g / mol) / (19,32 g / mL) = 10,19 mL / mol
Đó là, 1 mol nguyên tử vàng chiếm 10,19 mL, nhưng một nguyên tử vàng chiếm khối lượng cụ thể là bao nhiêu? Và làm thế nào để diễn đạt nó theo đơn vị chiều3? Đối với điều này chỉ đơn giản là áp dụng các yếu tố chuyển đổi sau đây:
(10,19 ml / mol) · (mol / 6.02 · 10)-23 nguyên tử) · (1 m / 100 cm)3· (1 giờ chiều / 10-12m)3= 16,92 · 106 chiều3
Mặt khác, bán kính nguyên tử của vàng là 166 pm. Nếu bạn so sánh cả hai khối lượng - khối lượng thu được bằng phương pháp trước đó và khối lượng được tính toán với công thức của khối lượng hình cầu - bạn sẽ thấy rằng chúng không có cùng giá trị:
VÂu= (4/3) (3.14) (166 chiều)3= 19,15 · 106 chiều3
Cái nào trong hai cái gần nhất với giá trị được chấp nhận? Kết quả gần nhất với kết quả thí nghiệm thu được từ nhiễu xạ tia X của cấu trúc tinh thể vàng.
Tài liệu tham khảo
- Helmenstine, Anne Marie, Tiến sĩ (Ngày 09 tháng 12 năm 2017). Định nghĩa khối lượng nguyên tử. Truy cập ngày 6 tháng 6 năm 2018, từ: thinkco.com
- Mayfair, Andrew. (Ngày 13 tháng 3 năm 2018). Cách tính thể tích của một nguyên tử. Khoa học. Truy cập ngày 6 tháng 6 năm 2018, từ: sciences.com
- Wiki Kids Ltd. (2018). Đường cong khối lượng nguyên tử Lothar Meyer. Truy cập ngày 6 tháng 6 năm 2018, từ: wonderwhizkids.com
- Lumen Xu hướng định kỳ: Bán kính nguyên tử. Truy cập ngày 6 tháng 6 năm 2018, từ: khóa học.lumenlearning.com
- Camilo J. Derpich. Khối lượng và mật độ nguyên tử. Truy cập ngày 6 tháng 6 năm 2018, từ: es-puraquimica.weebly.com
- Whites, Davis, Peck & Stanley. Hóa học (Tái bản lần thứ 8). Học tập CENGAGE, trang 222-224.
- Nền tảng CK-12. (Ngày 22 tháng 2 năm 2010). Kích thước nguyên tử so sánh. [Hình] Truy cập ngày 6 tháng 6 năm 2018, từ: commons.wikidia.org
- Nền tảng CK-12. (Ngày 22 tháng 2 năm 2010). Bán kính nguyên tử của H2. [Hình] Truy cập ngày 6 tháng 6 năm 2018, từ: commons.wikidia.org


