Cấu trúc, tính chất và công dụng của canxi oxit (CaO)
các canxi oxit (CaO) là một hợp chất vô cơ có chứa canxi và oxy ở dạng ion (không bị nhầm lẫn với canxi peroxide, CaO2). Nó được biết đến trên toàn thế giới là vôi, một từ chỉ định bất kỳ hợp chất vô cơ nào có chứa cacbonat, canxi oxit và hydroxit, cũng như các kim loại khác như silicon, nhôm và sắt..
Ôxít này (hoặc vôi) cũng được gọi chung là vôi vôi hoặc vôi tôi, tùy thuộc vào việc nó có ngậm nước hay không. Vôi là canxi oxit, trong khi vôi tôi là hydroxit của nó. Đổi lại, đá vôi (đá vôi hoặc vôi cứng) thực sự là một loại đá trầm tích có thành phần chủ yếu là canxi cacbonat (CaCO3).

Đây là một trong những nguồn canxi tự nhiên lớn nhất và tạo thành nguyên liệu thô để sản xuất canxi oxit. Oxit này được sản xuất như thế nào? Carbonate dễ bị phân hủy nhiệt; đốt nóng canxi cacbonat ở nhiệt độ trên 825 ° C, dẫn đến sự hình thành vôi và carbon dioxide.
Tuyên bố trên có thể được mô tả như sau: CaCO3(s) → CaO (s) + CO2(g) Bởi vì lớp vỏ trái đất rất giàu đá vôi và canxit, và trong các đại dương và bãi biển là vỏ sò biển (nguyên liệu thô để sản xuất canxi oxit), canxi oxit là thuốc thử tương đối rẻ.
Chỉ số
- 1 công thức
- 2 cấu trúc
- 3 thuộc tính
- 3.1 Độ hòa tan
- 4 công dụng
- 4.1 Làm vữa
- 4.2 Trong sản xuất kính
- 4.3 Trong khai thác
- 4.4 Là chất tẩy silicat
- 5 hạt nano oxit canxi
- 6 tài liệu tham khảo
Công thức
Công thức hóa học của canxi oxit là CaO, trong đó canxi giống như ion axit (chất nhận điện tử) Ca2+, và oxy là ion cơ bản (người cho điện tử) HOẶC2--.
Tại sao canxi có điện tích +2? Bởi vì canxi thuộc nhóm 2 của bảng tuần hoàn (ông Becambara) và chỉ có hai electron hóa trị có sẵn để hình thành liên kết, tạo ra nguyên tử oxy.
Cấu trúc
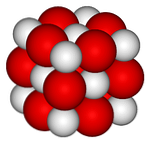
Trong hình trên, cấu trúc tinh thể (loại đá quý muối) cho canxi oxit được trình bày. Các quả cầu đỏ khổng lồ tương ứng với các ion Ca2+ và các quả cầu trắng cho các ion O2-.
Trong sắp xếp tinh thể khối này mỗi ion Ca2+ được bao quanh bởi sáu ion O2-, bị chặn lại trong các lỗ bát diện do các ion lớn để lại giữa chúng.
Cấu trúc này thể hiện tối đa tính chất ion của oxit này, mặc dù sự khác biệt đáng chú ý của bán kính (hình cầu màu đỏ lớn hơn màu trắng) tạo ra năng lượng hình lưới tinh thể yếu hơn khi so sánh với MgO.
Thuộc tính
Về mặt vật lý, nó là một chất rắn màu trắng tinh thể, không mùi và có tương tác tĩnh điện mạnh, chịu trách nhiệm cho các điểm nóng chảy cao (2572 ° C) và sôi (2850 ° C). Ngoài ra, nó có trọng lượng phân tử 55.958 g / mol và tính chất thú vị của sự phát quang.
Điều này có nghĩa là một mảnh canxi oxit tiếp xúc với ngọn lửa có thể tỏa sáng với ánh sáng trắng cực mạnh, được biết đến bằng tiếng Anh với tên gọi ánh đèn sân khấu, hoặc bằng tiếng Tây Ban Nha, ánh sáng của canxi. Các ion Ca2+, khi tiếp xúc với ngọn lửa, chúng gây ra ngọn lửa đỏ, như trong hình dưới đây.

Độ hòa tan
CaO là một oxit cơ bản có ái lực mạnh với nước, đến mức nó hấp thụ độ ẩm (nó là chất rắn hút ẩm), phản ứng ngay lập tức để tạo ra vôi hoặc canxi hydroxit.
CaO + s2O (l) => Ca (OH)2(s)
Phản ứng này tỏa nhiệt (giải phóng nhiệt) do sự hình thành của vật rắn có tương tác mạnh hơn và mạng tinh thể ổn định hơn. Tuy nhiên, phản ứng thuận nghịch nếu Ca (OH) được đun nóng2, khử nước và thắp sáng vôi tôi; sau đó, vôi "tái sinh".
Dung dịch thu được là rất cơ bản, và nếu nó được bão hòa bằng canxi oxit, nó sẽ đạt đến độ pH 12,8.
Tương tự như vậy, nó hòa tan trong glycerol và trong dung dịch axit và đường. Vì nó là một oxit cơ bản, tự nhiên nó có tương tác hiệu quả với các oxit axit (SiO2, Al2Ôi3 và đức tin2Ôi3, ví dụ) hòa tan trong các pha lỏng của chúng. Mặt khác, nó không hòa tan trong rượu và dung môi hữu cơ.
Công dụng
CaO có một số lượng lớn các ứng dụng công nghiệp, cũng như trong quá trình tổng hợp acetylene (CH≡CH), trong việc chiết xuất phốt phát từ nước thải và trong phản ứng với sulfur dioxide từ chất thải khí..
Các ứng dụng khác của canxi oxit được mô tả dưới đây:
Như một cái cối
Nếu canxi oxit được trộn với cát (SiO2) và nước, bánh với cát và phản ứng chậm với nước để tạo thành vôi tôi. Đổi lại, CO2 không khí hòa tan trong nước và phản ứng với muối để tạo thành canxi cacbonat:
Ca (OH)2(s) + CO2(g) => CaCO3(s) + H2Ô (l)
CaCO3 Nó là một hợp chất bền và cứng hơn CaO, làm cho vữa (hỗn hợp trước đó) cứng lại và cố định các viên gạch, khối hoặc gốm giữa chúng hoặc lên bề mặt mong muốn.
Trong sản xuất kính
Nguyên liệu thô cần thiết cho sản xuất kính là các oxit silic, được trộn với vôi, natri cacbonat (Na2CO3) và các chất phụ gia khác, sau đó được nung nóng, dẫn đến chất rắn thủy tinh. Chất rắn này sau đó được nung nóng và thổi trong bất kỳ số liệu nào.
Trong khai thác
Vôi tôi chiếm thể tích lớn hơn vôi sống do tương tác hydro (O - H - O). Tài sản này được sử dụng để phá vỡ các tảng đá từ bên trong.
Điều này đạt được bằng cách lấp đầy chúng bằng một hỗn hợp nhỏ gọn của vôi và nước, được niêm phong để tập trung nhiệt và sức mạnh mở rộng của nó trong đá.
Là một chất tẩy rửa silicat
CaO được hợp nhất với các silicat để tạo thành một chất lỏng kết hợp, sau đó được chiết xuất từ nguyên liệu thô của một sản phẩm nhất định.
Ví dụ, quặng sắt là nguyên liệu thô để sản xuất sắt kim loại và thép. Những khoáng chất này chứa silicat, là tạp chất không mong muốn cho quá trình và được loại bỏ bằng phương pháp vừa mô tả.
Hạt nano oxit canxi
Canxi oxit có thể được tổng hợp dưới dạng hạt nano, thay đổi nồng độ canxi nitrat (Ca (NO3)2) và natri hydroxit (NaOH) trong dung dịch.
Những hạt này có dạng hình cầu, cơ bản (cũng như chất rắn ở quy mô vĩ mô) và có nhiều diện tích bề mặt. Do đó, các tính chất này có lợi cho các quá trình xúc tác. Cái nào? Các cuộc điều tra hiện đang trả lời câu hỏi đó.
Các hạt nano này đã được sử dụng để tổng hợp các hợp chất hữu cơ thay thế - có nguồn gốc từ pyridin - trong công thức của các loại thuốc mới để thực hiện các biến đổi hóa học như quang hợp nhân tạo, để làm sạch nước từ các kim loại nặng và độc hại, và như tác nhân xúc tác quang.
Các hạt nano có thể được tổng hợp trên một hỗ trợ sinh học, chẳng hạn như lá đu đủ và trà xanh, được sử dụng như một tác nhân kháng khuẩn.
Tài liệu tham khảo
- scifun.org (2018). Vôi: canxi oxit. Truy cập ngày 30 tháng 3 năm 2018, từ: scifun.org.
- Wikipedia. (2018). Canxi oxit. Truy cập ngày 30 tháng 3 năm 2018, từ: en.wikipedia.org
- Ashwini Anantharaman et al. (2016). Tổng hợp màu xanh lá cây của hạt nano oxit canxi và ứng dụng của nó. Tạp chí Nghiên cứu Kỹ thuật và Ứng dụng. ISSN: 2248-9622, Tập 6, Số 10, (Phần -1), tr.27-31.
- J. Safaei-Ghomi et al. (2013). Các hạt nano oxit canxi xúc tác tổng hợp đa thành phần một bước của pyridin được thay thế cao trong môi trường ethanol nước Khoa học Iranica, Giao dịch C: Kỹ thuật hóa học và hóa học 20 549-554.
- PubChem. (2018). Canxi Oxit. Truy cập ngày 30 tháng 3 năm 2018, từ: pubool.ncbi.nlm.nih.gov
- Rùng mình & Atkins. (2008). Hóa vô cơ Trong Các yếu tố của nhóm 2. (ấn bản thứ tư, trang 280). Đồi Mc Graw.


