Đặc điểm proteinase K, hoạt động enzyme và ứng dụng
các proteinase K là một enzyme thuộc nhóm protease serine, nghĩa là, nó có ở trung tâm xúc tác hoạt động của nó là một serine axit amin và có chức năng phá vỡ các liên kết peptide bằng cách thủy phân. Đổi lại, enzyme này thuộc họ protein Subilisin (peptidase S8).
Proteinase K có trọng lượng phân tử (MW) là 28.900 dalton và được phân lập lần đầu tiên vào năm 1974 từ chiết xuất của nấm Album Engyodontium, trước đây được biết đến với tên của Album Tritirachium Limber.
Nó thể hiện khả năng phân giải protein cao, được chứng minh là có thể làm giảm chất keratin có trong tóc. Từ keratin trong tiếng Anh được viết là "keratin", do đó nó được gọi là "proteinase K".
Do khả năng cao để tách protein bản địa, enzyme này rất hữu ích trong các kỹ thuật sinh học phân tử khác nhau. Nó chủ yếu được sử dụng để cô lập và điều chế axit nucleic có trọng lượng phân tử cao (MW).
Proteinase K hoạt động bằng cách giải phóng DNA hạt nhân, đồng thời phá hủy protein và làm bất hoạt RNase và DNase, nghĩa là loại bỏ các nuclease trong chế phẩm DNA và RNA..
Mặt khác, người ta đã thấy rằng proteinase K có thể thủy phân một số protein bản địa bị biến tính, điều này đã làm dấy lên sự quan tâm của các nhà nghiên cứu về việc sử dụng nó trong nghiên cứu về protein prion (PrPC).
Tuy nhiên, mặc dù khả năng phân giải protein cao, vẫn có những protein kháng lại tác dụng của proteinase K. Trong số này, có một số protein bất thường được gọi là prion (PrPSc), liên quan đến bệnh não xốp dạng xốp truyền.
Chỉ số
- 1 Đặc điểm của proteinase K
- 2 hoạt động enzyme
- 3 ứng dụng
- 4 Ưu điểm của proteinase K
- 5 protein kháng proteinase K
- 6 tài liệu tham khảo
Đặc điểm của proteinase K
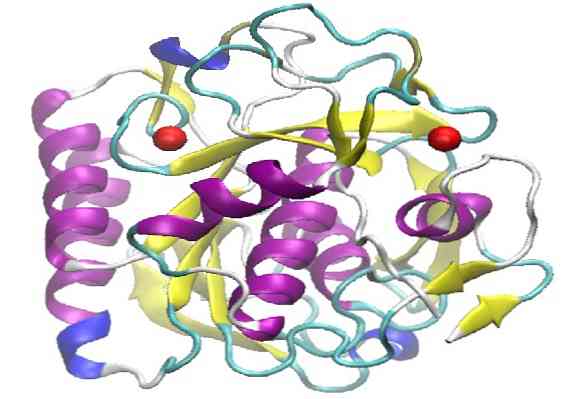
Proteinase K có một cấu trúc đại học bao gồm ba lớp, với một tấm β inmiscuidas Bảy chuỗi giữa hai lớp xoắn. Thuộc về gia đình của peptidase S8 được đặc trưng bởi vị trí hoạt động của mình trong một bộ ba xúc tác, có thứ tự tuần tự là (Asp, Ngài và Ser), mà phân biệt chúng từ các gia đình peptidase khác.
Enzyme này từ nhóm protease serine được đặc trưng bằng cách thủy phân các liên kết peptide gần với nhóm carboxylic của axit amin aliphatic và thơm.
Mặt khác, nó có thể hoạt động với sự có mặt của một số chất ăn mòn, chẳng hạn như natri dodecyl sulfate (SDS), Tris-HCL và EDTA, được sử dụng để giúp làm biến tính protein, khiến chúng mất cấu trúc tự nhiên.
Đây là bước đầu tiên trong quá trình chuẩn bị protein cho kỹ thuật điện di. Phạm vi pH mà tại đó proteinase K hoạt động khá rộng (2.0 đến 12.0), với độ pH tối ưu trong khoảng từ 7.5 đến 12.0 và điểm đẳng điện của nó là 8,9. Như có thể thấy, nó hoạt động chống lại phạm vi pH rất rộng.
Một đặc điểm khác nổi bật trong proteinase K là tính ổn định của nó khi có nhiệt độ cao (50 - 60 ° C).
Hoạt động men
Proteinase K cần sự hiện diện của ion canxi, mặc dù điều này không ảnh hưởng đến hoạt động của nó, nếu cần thiết để duy trì sự ổn định của nó.
Để proteinase K thực hiện quá trình tiêu hóa hoàn toàn cơ chất, cần có thời gian tiếp xúc gần đúng trong khoảng từ 5 phút đến 2 giờ.
Tuy nhiên, theo nghĩa này, Daza và cộng sự đã so sánh độ tinh khiết của DNA thu được ở nhiều lần tiếp xúc với proteinase K và kết luận rằng việc ủ bệnh kéo dài (lên đến 24 giờ) giúp cải thiện đáng kể chất lượng DNA.
Bây giờ, liên quan đến nồng độ được sử dụng của enzyme proteinase K trong các giao thức khác nhau, có thể nói rằng nó rất đa dạng.
Nó có thể được sử dụng từ nồng độ rất thấp (5 g / ml) đến nồng độ 500 g / ml. Nhưng nồng độ công việc thường xuyên nhất nằm trong khoảng từ 50-100μg / ml, đặc biệt đối với quá trình tiêu hóa protein và bất hoạt nuclease. Mặc dù nồng độ 2 mg / ml là cần thiết để điều trị mô.
Ứng dụng
Các ứng dụng của nó rất rộng và có thể được tóm tắt như sau:
-Nó được sử dụng trong tiêu hóa protein và chiết xuất DNA bằng một số phương pháp như: khử muối, PK-SDS, cetyl-trimethyl ammonium bromide (CTAB), kali axetat biến đổi và chiết xuất bằng natri iodua..
-Bất hoạt các nuclease (RNase và DNase).
-Trong kỹ thuật lai tại chỗ (NGÀI), để giúp giải phóng axit nucleic, ngoài việc loại bỏ các protein không mong muốn.
-Điều chỉnh protein.
-Ở cấp độ nghiên cứu, trong các nghiên cứu khác nhau.
Ưu điểm của proteinase K
Đã có nhiều nghiên cứu so sánh các kỹ thuật tách chiết DNA sử dụng proteinase K, với những người khác không được sử dụng và tất cả các kết luận rằng có là lớn nhất khi enzyme được sử dụng. Trong số những lợi thế chúng ta có thể kể đến như sau:
-DNA trọng lượng phân tử cao có chất lượng cao và độ tinh khiết thu được.
-DNA chiết xuất ổn định đến 3 tháng.
DNA chiết xuất có thể được sử dụng trong các kỹ thuật sau: Nam blot, phản ứng chuỗi polymerase (PCR), điện di, trong số các kỹ thuật khác.
Protein kháng proteinase K
Các cuộc điều tra khác nhau đã kết luận rằng prion (protein độc hại PrPSc bất thường) được phân biệt với protein PrPC (bản địa) vì chúng chống lại tác động của proteinase K, trong khi PrPC nhạy cảm với hành động của chúng.
Các tác giả khác đã mô tả rằng trong cấu trúc của PrPSc có những phần nhạy cảm và những phần khác kháng với proteinase K. Tuy nhiên, cả hai phần đều độc hại và nhiễm trùng như nhau..
Mặt khác, Bastian và cộng tác viên năm 1987 đã phân lập 4 protein gồm 28, 30, 66 và 76 kda từ một loài Spiroplasma mirum. Tất cả đều kháng lại tác dụng của proteinase K và cũng có phản ứng chéo với một số prion.
Được biết, loài này có thể gây đục thủy tinh thể và tổn thương thần kinh quan trọng và do những phát hiện khoa học của Bastian, trong số các nghiên cứu khác, một nỗ lực đã được thực hiện để liên kết vi sinh vật này với bệnh não xốp truyền bệnh.
Tuy nhiên, nguyên nhân của bệnh lý thần kinh thoái hóa này vẫn được quy cho prion ngày nay.
Theo nghĩa này, Butler và cộng tác viên vào năm 1991 đã xác định và mô tả một lớp protein K kháng protein 40 Kda từ hai chủng Mycoplasma hyorhinis. Tác nhân gây bệnh này ảnh hưởng đến lợn, lây nhiễm vào các mô của chúng, nhưng trong trường hợp này không có phản ứng chéo với các prion đã được thử nghiệm.
Cần nhiều nghiên cứu hơn để làm sáng tỏ nhiều điều chưa biết về nó.
Tài liệu tham khảo
- Bastian F, Jennings R và Gardner W. 1987. Antiserum đối với phản ứng chéo protein fibril liên quan đến phế liệu với Spiroplasma mirum protein fibril. J. Lâm sàng. Microbiol. 25: 2430-2431.
- Daza C, Guillen J, King J, Ruiz V. Đánh giá phương pháp chiết tách và tinh lọc DNA từ mô cơ cố định trong formaldehyd từ xác chết không xác định. Tạp chí Med, 2014; 22 (1): 42-49,
- Butler G, Kotani H, Kong L, Frick M, Evancho S, Stanbridge E, và Mcgarrity G. Nhận dạng và đặc tính của các protein kháng K proteinase trong các thành viên của động vật thân mềm. Nhiễm trùng và miễn dịch, 1991, 59 (3): 1037-1042
- López M, Rivera M, Viettri M, Lares M, Morocoima A, Herrera L, et al. So sánh hai giao thức trích xuất DNA từ Trypanosoma cruzi trồng trong môi trường axen. Mục sư Peru. Trung tâm y tế công cộng 2014; 31 (2): 222-227. Có sẵn tại: scielo.org
- Jiménez G, Villalobos M, Jiménez E và Palma W. Xác định hiệu quả của năm giao thức trích xuất DNA từ vật liệu parafin cho các nghiên cứu phân tử. Rev Méd Univ Costa Rica. 2007; 1 (1): 10-19.


