Cấu trúc, tính chất và công dụng của Butino
các butino là một hợp chất hóa học thuộc nhóm alkynes, được đặc trưng chủ yếu bằng cấu trúc của nó ít nhất là liên kết ba giữa hai nguyên tử carbon.
Khi nói đến việc thiết lập các quy tắc về mệnh giá của alkynes, IUPAC (từ viết tắt trong tiếng Anh của International Union of Pure and Application Chemistry) đã xác định rằng chúng được sử dụng giống như cho anken.

Sự khác biệt cơ bản giữa danh pháp của cả hai loại chất là hậu tố -one được đổi thành -hoặc khi nói đến các hợp chất có liên kết ba trong cấu trúc của nó.
Mặt khác, butino chỉ bao gồm carbon và hydro, và nó có hai dạng: 1-butyne, ở pha khí trong điều kiện áp suất và nhiệt độ tiêu chuẩn (1 atm, 25 ° C); và 2-butino, một loại pha lỏng được tạo ra bởi quá trình tổng hợp hóa học.
Chỉ số
- 1 Cấu trúc hóa học
- 1.1 1-butino
- 1.2 2-butyne
- 2 thuộc tính
- 3 công dụng
- 4 tài liệu tham khảo
Cấu trúc hóa học
Trong phân tử được gọi là butino, hiện tượng đồng phân cấu trúc của vị trí được trình bày, bao gồm sự hiện diện của các nhóm chức giống nhau trong cả hai hợp chất, nhưng mỗi phân tử này ở một vị trí khác nhau của chuỗi.
Trong trường hợp này, cả hai dạng butino đều có công thức phân tử giống hệt nhau; tuy nhiên, trong 1-butyne, liên kết ba được đặt ở carbon số một, trong khi ở 2-butyne, nó được tìm thấy ở số hai. Điều này chuyển đổi chúng thành các đồng phân vị trí.
Do vị trí của liên kết ba trong một trong các thiết bị đầu cuối của cấu trúc 1-butyne, nó được coi là một alkyne cuối, trong khi vị trí trung gian của liên kết ba trong cấu trúc 2-butyne cho phép phân loại alkyne bên trong.
Do đó, liên kết chỉ có thể nằm giữa carbon thứ nhất và thứ hai (1-butyne) hoặc giữa carbon thứ hai và thứ ba (2-butyne). Điều này là do danh pháp được áp dụng, trong đó việc đánh số thấp nhất có thể sẽ luôn được trao cho vị trí liên kết ba.
1-butino
Hợp chất có tên 1-butyne còn được gọi là ethylacetylene, vì cấu trúc của nó và cách thức mà bốn nguyên tử carbon của nó được sắp xếp và liên kết. Tuy nhiên, khi nói về butino tài liệu tham khảo chỉ được thực hiện cho loài hóa chất này.
Trong phân tử này, liên kết ba được tìm thấy trong một carbon cuối, cho phép sự có sẵn của các nguyên tử hydro mang lại cho nó khả năng phản ứng tuyệt vời.
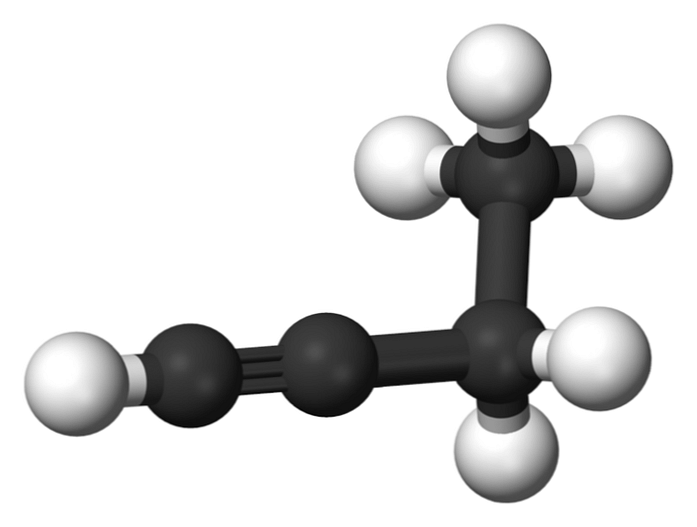
Liên kết cứng và mạnh hơn liên kết đơn hoặc đôi giữa các nguyên tử carbon này cung cấp cấu hình ổn định của hình học tuyến tính 1-butyne.
Mặt khác, chất khí này khá dễ cháy, do đó, khi có nhiệt, nó có thể gây ra các vụ cháy hoặc nổ dễ dàng và có khả năng phản ứng lớn khi có không khí hoặc nước.
2-butyne
Vì alkynes bên trong thể hiện sự ổn định cao hơn alkynes cuối, chúng cho phép biến đổi 1-butyne thành 2-butyne.
Quá trình đồng phân hóa này có thể xảy ra bằng cách đun nóng 1-butyne với sự có mặt của một bazơ (như NaOH, KOH, NaOCH3 ...) hoặc thông qua việc sắp xếp lại 1-butyne trong dung dịch kali hydroxit (KOH) trong ethanol (C2H6Ô).
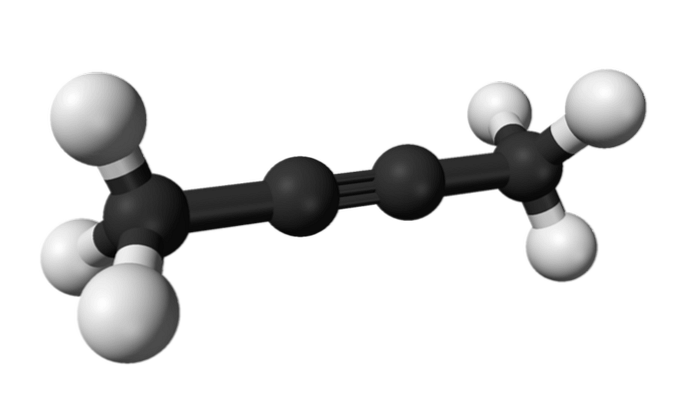
Theo cách tương tự, hóa chất có tên là 2-butyne còn được gọi là dimethylacetylene (hay crotonylene), hiện diện như một loại chất lỏng và dễ bay hơi có nguồn gốc nhân tạo.
Trong 2-butyne, liên kết ba nằm ở giữa phân tử, tạo cho nó sự ổn định cao hơn so với đồng phân của nó.
Ngoài ra, hợp chất không màu này có mật độ thấp hơn nước mặc dù nó được coi là không hòa tan trong nó và có tính dễ cháy cao.
Thuộc tính
-Công thức cấu tạo của butino (bất kể đồng phân nào được tham chiếu) là C4H6, trong đó có cấu trúc tuyến tính.
-Một trong những phản ứng hóa học mà phân tử butine phải chịu là sự đồng phân hóa, trong đó sự sắp xếp lại và di chuyển của liên kết ba xảy ra trong phân tử.
-1-Butyne đang trong pha khí, có tính dễ cháy rất cao và mật độ cao hơn không khí.
-Chất này cũng khá phản ứng và khi có nhiệt có thể gây nổ dữ dội.
-Ngoài ra, khi khí không màu này trải qua phản ứng đốt cháy không hoàn toàn, nó có thể gây ra carbon monoxide (CO)
-Khi cả hai đồng phân tiếp xúc với nhiệt độ cao, chúng có thể gặp phản ứng trùng hợp kiểu nổ.
-2-butyne đang ở pha lỏng, mặc dù nó cũng được coi là khá dễ cháy trong điều kiện áp suất và nhiệt độ tiêu chuẩn.
-Các chất này có thể gặp phản ứng dữ dội khi chúng có mặt các chất oxy hóa mạnh.
-Theo cách tương tự, các phản ứng tỏa nhiệt với sự giải phóng hậu quả của khí hydro xảy ra khi có sự hiện diện của các loài khử..
-Khi tìm thấy tiếp xúc với một số chất xúc tác nhất định (như một số chất có tính axit) hoặc các loài khởi động, các phản ứng trùng hợp loại tỏa nhiệt có thể xảy ra.
Công dụng
Vì chúng có một số tính chất khác nhau, cả hai đồng phân có thể có cách sử dụng và ứng dụng khác nhau, như được hiển thị bên dưới:
Ở nơi đầu tiên, rất thường là một trong những ứng dụng của 1-butino là việc sử dụng nó như là một giai đoạn trung gian trong quy trình sản xuất các chất khác có bản chất hữu cơ có nguồn gốc tổng hợp..
Mặt khác, loài hóa chất này được sử dụng trong ngành sản xuất cao su và các hợp chất có nguồn gốc; ví dụ như khi bạn muốn lấy benzol.
Tương tự, nó được sử dụng trong quá trình sản xuất nhiều loại sản phẩm nhựa, cũng như trong sản xuất nhiều chất polyetylen được coi là mật độ cao.
Ngoài ra, 1-butyne thường được sử dụng làm thành phần cho các quá trình cắt và hàn của một số hợp kim kim loại, bao gồm thép (hợp kim sắt và carbon)..
Theo một nghĩa khác, đồng phân 2 butyne được sử dụng kết hợp với một alkyne khác gọi là propyne trong quá trình tổng hợp một số chất gọi là hydroquinone kiềm hóa, khi quá trình tổng hợp α-tocopherol (vitamin E) được thực hiện.
Tài liệu tham khảo
- Wikipedia. (s.f.). Butyne Lấy từ en.wikipedia.org
- Yoder, C. H., Leber P. A. và Thomsen, M. W. (2010). Cầu nối hóa học hữu cơ: Khái niệm và danh pháp. Lấy từ sách.google.com.vn
- Học tập.com. (s.f.). Butyne: Công thức cấu trúc & đồng phân. Có được từ nghiên cứu.
- PubChem. (s.f.). 1-Butyne. Lấy từ pubool.ncbi.nlm.nih.gov
- PubChem. (s.f.). 2-Butyne. Lấy từ pubool.ncbi.nlm.nih.gov


