Tính chất, rủi ro và công dụng của Hydrogen Sulfide (H2S)
các hydro sunfua là tên gọi chung của hydro sunfua (H2S). Nó có thể được coi là một axit hydrazide trong dung dịch (H2S (aq)).
Việc xem xét axit sulfhydryl được đưa ra mặc dù độ hòa tan thấp trong nước của hợp chất hóa học này. Cấu trúc của nó được trình bày trong hình 1 (EMBL-EBI, 2005).
Do đó, hydro sunfua ít tan trong nước. Khi hòa tan nó tạo thành ion axit sunfua hoặc hydrosulfide (HS-). Dung dịch nước của hydro sunfua, hoặc hydro sunfua, không màu và khi tiếp xúc với không khí, oxy hóa chậm lưu huỳnh nguyên tố, không tan trong nước.
Lưu huỳnh lưu huỳnh S2- nó chỉ tồn tại trong dung dịch nước kiềm mạnh; Nó đặc biệt cơ bản với pKa> 14.
H2S phát sinh từ hầu như nơi lưu huỳnh nguyên tố tiếp xúc với vật liệu hữu cơ, đặc biệt là ở nhiệt độ cao. Hydrogen sulfide là một hydride cộng hóa trị liên quan đến hóa học (H2O), vì oxy và lưu huỳnh được sản xuất trong cùng một nhóm với bảng tuần hoàn.
Nó thường có kết quả khi vi khuẩn phân hủy chất hữu cơ trong trường hợp không có oxy, chẳng hạn như trong đầm lầy và cống rãnh (cùng với quá trình tiêu hóa kỵ khí). Nó cũng xảy ra trong khí núi lửa, khí tự nhiên và một số vùng nước giếng.
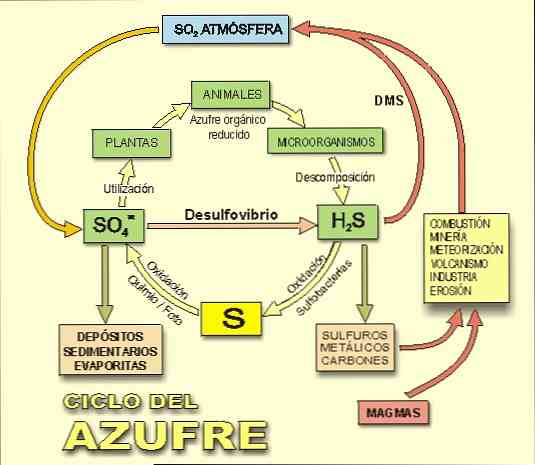
Cũng cần lưu ý rằng hydro sunfua là thành phần trung tâm trong chu trình lưu huỳnh, chu trình hóa sinh của lưu huỳnh trên Trái đất (hình 2).
Như đã đề cập ở trên, vi khuẩn khử lưu huỳnh và khử sunfat thu được năng lượng oxy hóa từ hydro hoặc các phân tử hữu cơ khi không có oxy bằng cách khử lưu huỳnh hoặc sunfat thành hydro sunfua.
Các vi khuẩn khác giải phóng hydro sunfua từ các axit amin có chứa lưu huỳnh. Một số nhóm vi khuẩn có thể sử dụng hydro sunfua làm nhiên liệu, oxy hóa nó thành lưu huỳnh nguyên tố hoặc sunfat sử dụng oxy hoặc nitrat làm chất oxy hóa.
Vi khuẩn lưu huỳnh tinh khiết và vi khuẩn lưu huỳnh màu xanh lá cây sử dụng hydro sunfua làm chất cho điện tử trong quá trình quang hợp, do đó tạo ra lưu huỳnh nguyên tố.
Trên thực tế, chế độ quang hợp này cũ hơn chế độ của vi khuẩn lam, tảo và thực vật sử dụng nước làm chất cho điện tử và giải phóng oxy (Cơ sở dữ liệu chuyển hóa của con người, 2017).
Chỉ số
- 1 Trường hợp hydro sunfua được sản xuất?
- 2 Tính chất lý hóa
- 3 Phản ứng và mối nguy hiểm
- 3.1 Hít phải
- 3.2 Tiếp xúc với da
- 3.3 Giao tiếp bằng mắt
- 4 công dụng
- 4.1 1- Sản xuất lưu huỳnh
- 4.2 2- Hóa phân tích
- 4.3 3- Công dụng khác
Nơi sản xuất hydro sunfua?
Hydrogen sulfide (H2S) xảy ra tự nhiên trong dầu thô, khí tự nhiên, khí núi lửa và suối nước nóng. Nó cũng có thể là kết quả của sự xuống cấp vi khuẩn của chất hữu cơ. Nó cũng được sản xuất bởi chất thải của con người và động vật.
Vi khuẩn được tìm thấy trong miệng và đường tiêu hóa sản xuất hydro sunfua từ vi khuẩn phá vỡ các vật liệu có chứa protein thực vật hoặc động vật.
Hydrogen sulfide cũng có thể là kết quả của các hoạt động công nghiệp, như chế biến thực phẩm, lò luyện cốc, nhà máy giấy kraft, xưởng thuộc da và nhà máy lọc dầu (Cơ quan đăng ký chất độc và bệnh tật, 2011).
Tính chất hóa lý
Hydrogen sulfide là một loại khí không màu với mùi trứng thối mạnh. Dung dịch nước của hydro sunfua không màu mà không có mùi thơm đặc trưng.
Hợp chất có trọng lượng phân tử 34,1 g / mol, dung dịch nước có mật độ 1,43 g / ml. Nó có điểm nóng chảy là -82 ° C và điểm sôi là -60 ° C. Nó ít tan trong nước, có thể hòa tan chỉ 4 gram mỗi lít dung môi này ở 20 ° C (Hiệp hội Hóa học Hoàng gia, 2015).
Hydrogen sulfide phản ứng như một axit và như một chất khử. Nó phát nổ khi tiếp xúc với oxy differluoride, brom pentafluoride, clo trifluoride, dichloride oxide và bạc Fulminate. Nó có thể bốc cháy và phát nổ khi tiếp xúc với bột đồng, với sự có mặt của oxy.
Nó có thể phản ứng theo cách tương tự với các kim loại bột khác. Nó được đốt cháy khi tiếp xúc với oxit kim loại và peroxit (bari peroxide, crom trioxide, đồng oxit, chì dioxide, mangan dioxide, oxit niken, oxit bạc, bạc dioxide, thallium trioxide, natri peroxide, oxit thủy ngân, oxit canxi).
Nó được đốt cháy bằng bạc bromate, chì (II) hypochlorite, cromat đồng, axit nitric, oxit chì (IV) và oxit. Nó có thể bốc cháy nếu đi qua các ống sắt gỉ. Phản ứng tỏa nhiệt với các bazơ.
Nhiệt của phản ứng với vôi soda, natri hydroxit, kali hydroxit, bari hydroxit có thể gây cháy hoặc nổ phần không phản ứng khi có không khí / oxy (HYDROGEN SULFIDE, 2016).
Tính phản ứng và mối nguy hiểm
H2S được coi là một hợp chất ổn định mặc dù nó rất dễ cháy và cực kỳ độc hại.
Hợp chất này nặng hơn không khí và có thể di chuyển một khoảng cách đáng kể đến nguồn đánh lửa và sao lưu. Có thể tạo thành hỗn hợp nổ với không khí trong một phạm vi rộng.
Nó cũng phản ứng bùng nổ với pentafluoride brom, clo trifluoride, nitơ triiodide, nitơ trichloride, oxy differluoride và phenyl diazonium clorua.
Khi được đun nóng để phân hủy, nó thải ra khói oxit lưu huỳnh cực độc. Không tương thích với nhiều vật liệu bao gồm các chất oxy hóa mạnh, kim loại, axit nitric mạnh, pentafluoride brom, clo trifluoride, nitơ triiodide, nitơ trichloride, oxy differluoride và phenyl diazonium clorua.
Hydrogen sulfide (H2S) chịu trách nhiệm cho nhiều sự cố phơi nhiễm độc hại nghề nghiệp, đặc biệt là trong ngành dầu khí. Tác dụng lâm sàng của H2S phụ thuộc vào nồng độ của nó và thời gian tiếp xúc.
H2S gây tử vong ngay lập tức khi nồng độ hơn 500-1000 phần triệu (ppm), nhưng tiếp xúc với nồng độ thấp hơn, chẳng hạn như 10-500 ppm, có thể gây ra các triệu chứng hô hấp khác nhau, từ viêm mũi đến suy hô hấp cấp.
H2S cũng có thể ảnh hưởng đến nhiều cơ quan, gây ra các rối loạn tạm thời hoặc vĩnh viễn trong hệ thống thần kinh, tim mạch, thận, gan và huyết học.
Một trường hợp phơi nhiễm nghề nghiệp với H được trình bày2S dẫn đến sự tham gia của một số cơ quan, suy hô hấp cấp tính, tổ chức viêm phổi và sốc tương tự như nhiễm trùng huyết cấp tính. Trong trường hợp này, bệnh nhân cũng bị bệnh phổi tắc nghẽn và hạn chế nhẹ và bệnh lý thần kinh ngoại biên (Al-Tawfiq, 2010).
Hít phải
Trong trường hợp hít phải, hãy mang nó ra ngoài trời và giữ cho nó nghỉ ngơi ở một vị trí thoải mái để thở. Nếu không thở, quản lý hô hấp nhân tạo. Nếu thở khó khăn, nhân viên được đào tạo nên cung cấp oxy.
Tiếp xúc với da
Trong trường hợp tiếp xúc với da, cần rửa sạch với nhiều nước. Chất lỏng điều áp có thể gây tê cóng. Trong trường hợp tiếp xúc với chất lỏng có áp suất, vùng đóng băng phải được làm nóng ngay lập tức với nước ấm không quá 41 ° C.
Nhiệt độ của nước phải chịu được với da bình thường. Làm ấm da nên được duy trì trong ít nhất 15 phút hoặc cho đến khi màu sắc và cảm giác bình thường trở lại khu vực bị ảnh hưởng. Trong trường hợp tiếp xúc nhiều, quần áo được cởi ra trong khi tắm bằng nước ấm.
Giao tiếp bằng mắt
Trong trường hợp tiếp xúc với mắt, rửa mắt kỹ bằng nước trong ít nhất 15 phút. Giữ cho mí mắt mở và tránh xa nhãn cầu để đảm bảo tất cả các bề mặt được rửa kỹ.
Nuốt phải không được coi là một lộ trình có thể tiếp xúc. Đối với tất cả các trường hợp khác, phải có sự chăm sóc y tế ngay lập tức (Praxair, 2016).
Công dụng
1- Sản xuất lưu huỳnh
Một đơn vị thu hồi lưu huỳnh Claus bao gồm lò đốt, nồi hơi thải nhiệt, bình ngưng lưu huỳnh và một loạt các giai đoạn xúc tác, mỗi giai đoạn sử dụng quá trình hâm nóng, lớp xúc tác và bình ngưng lưu huỳnh. Thông thường, hai hoặc ba giai đoạn xúc tác được sử dụng.
Quá trình Claus chuyển đổi hydro sunfua thành lưu huỳnh nguyên tố thông qua phản ứng hai bước.
Giai đoạn đầu tiên liên quan đến quá trình đốt cháy có kiểm soát của khí nạp để chuyển đổi khoảng một phần ba hydro sunfua thành lưu huỳnh đioxit và phản ứng không xúc tác của hydro sunfua không được đốt cháy bằng sulfur dioxide.
Trong giai đoạn thứ hai, phản ứng Claus, hydro sunfua và lưu huỳnh đioxit phản ứng với chất xúc tác để tạo ra lưu huỳnh và nước.
Lượng không khí đốt được kiểm soát chặt chẽ để tối đa hóa thu hồi lưu huỳnh, nghĩa là duy trì phản ứng cân bằng hóa học của hydro sunfua 2: 1 với lưu huỳnh đioxit thông qua các lò phản ứng xuôi dòng.
Thông thường, có thể thu hồi lưu huỳnh tới 97% (Thư viện Y khoa Quốc gia Hoa Kỳ, 2011).
2- Hóa phân tích
Trong hơn một thế kỷ, hydro sunfua rất quan trọng trong hóa học phân tích, trong phân tích vô cơ định tính các ion kim loại.
Trong các phân tích này, các ion kim loại nặng (và phi kim loại) bị kết tủa (ví dụ: Pb (II), Cu (II), Hg (II), As (III) từ dung dịch sau khi tiếp xúc với H2S. Kết tủa thu được hòa tan trở lại với một số chọn lọc và do đó được xác định.
3- Công dụng khác
Hợp chất này cũng được sử dụng để tách oxit deuterium, hoặc nước nặng từ nước bình thường thông qua quá trình Girdler sulfide.
Các nhà khoa học tại Đại học Exeter đã phát hiện ra rằng tế bào tiếp xúc với một lượng nhỏ khí hydro sunfua có thể ngăn ngừa tổn thương ty thể.
Khi tế bào bị căng thẳng với bệnh, các enzyme bị thu hút vào tế bào để tạo ra một lượng nhỏ hydro sunfua. Nghiên cứu này có thể có nhiều ý nghĩa hơn trong việc ngăn ngừa đột quỵ, bệnh tim và viêm khớp (Stampler, 2014).
Hydrogen sulfide có thể có đặc tính chống lão hóa bằng cách ngăn chặn các hóa chất phá hủy trong tế bào, có đặc tính tương tự resveratrol, một chất chống oxy hóa có trong rượu vang đỏ.
Tài liệu tham khảo
- Cơ quan Quản lý Chất độc và Đăng ký Bệnh. (2011, ngày 3 tháng 3). Hydrogen Sulfide Carbonyl Sulfide. Lấy từ atsdr.cdc.gov.
- Al-Tawfiq, B. D. (2010). Phơi nhiễm hydro sunfua ở nam giới trưởng thành. Biên niên sử của Ả Rập Saudi 30 (1) , 76-80.
- EMBL-EBI (2005, ngày 13 tháng 12). hydro sunfua. Phục hồi từ ebi.ac.uk.
- bách khoa toàn thư britannica. (S.F.). Hydrogen sunfua. Phục hồi từ britannica.com.
- Cơ sở dữ liệu trao đổi chất của con người. (2017, ngày 2 tháng 3). Hydrogen sunfua . Lấy từ hmdb.ca.
- HY SINH. (2016). Lấy từ cameochemicals.noaa.gov.
- (2016, ngày 17 tháng 10). Bảng dữ liệu an toàn hydro sunfua. Phục hồi từ Praxair.com.
- Hội hóa học hoàng gia. (2015). Hydrogen sunfua. Lấy từ chemspider.com.
- Stampler, L. (2014, 11 tháng 7). Một hợp chất hôi thối có thể bảo vệ chống lại tổn thương tế bào, nghiên cứu tìm thấy. Lấy từ time.com.
- S. Thư viện Y khoa Quốc gia. (2011, ngày 22 tháng 9). Lưu huỳnh, nguyên tố. Lấy từ toxnet.nlm.nih.gov.


