Cấu trúc, tính chất, danh pháp của bạc sunfua (Ag2S)
các bạc sunfua là một hợp chất vô cơ có công thức hóa học là Ag2S. Nó bao gồm một chất rắn màu xám đen được hình thành bởi các cation Ag+ và anion S2- theo tỷ lệ 2: 1. S2- nó rất giống với Ag+, bởi vì cả hai đều là các ion mềm và chúng có thể ổn định với nhau.
Đồ trang trí bạc có xu hướng tối, mất ánh sáng đặc trưng của họ. Sự thay đổi màu sắc không phải là sản phẩm của quá trình oxy hóa bạc, mà là phản ứng của nó với hydro sunfua có trong môi trường ở nồng độ thấp; Điều này có thể đến từ sự thối rữa hoặc suy thoái của thực vật, động vật hoặc thực phẩm giàu lưu huỳnh.

H2S, có phân tử mang nguyên tử lưu huỳnh, phản ứng với bạc theo phương trình hóa học sau: 2Ag (s) + H2S (g) => Ag2S (s) + H2(g)
Do đó, Ag2S chịu trách nhiệm cho các lớp màu đen hình thành trên bạc. Tuy nhiên, trong tự nhiên lưu huỳnh này cũng có thể được tìm thấy trong các khoáng chất acantita và argentita. Hai khoáng chất được phân biệt với nhiều loại khác bởi các tinh thể màu đen và sáng của chúng, giống như chất rắn trong hình trên.
Ag2S trình bày các cấu trúc đa hình, các tính chất điện tử và quang điện tử hấp dẫn, là chất bán dẫn và hứa hẹn sẽ là vật liệu để phát triển các thiết bị quang điện, như pin mặt trời.
Chỉ số
- 1 cấu trúc
- 2 thuộc tính
- 2.1 Trọng lượng phân tử
- 2.2 Ngoại hình
- 2.3 Mùi
- 2.4 Điểm nóng chảy
- 2.5 Độ hòa tan
- Cấu trúc 2.6
- 2.7 Chỉ số khúc xạ
- Hằng số điện môi 2.8
- 2.9 Điện tử
- 2.10 Phản ứng khử
- 3 danh pháp
- 3.1 Hệ thống
- 3.2 Cổ phiếu
- 3.3 Truyền thống
- 4 công dụng
- 5 tài liệu tham khảo
Cấu trúc
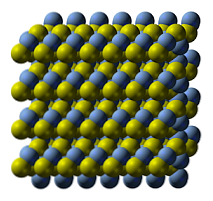
Cấu trúc tinh thể của bạc sunfua được minh họa trong hình trên. Các quả cầu màu xanh tương ứng với các cation Ag+, trong khi những cái màu vàng cho anion S2-. Ag2S là đa hình, có nghĩa là nó có thể áp dụng một số hệ tinh thể trong điều kiện nhiệt độ nhất định.
Thế nào? Thông qua một giai đoạn chuyển tiếp. Các ion được sắp xếp lại theo cách sao cho sự tăng nhiệt độ và các dao động của vật rắn không làm ảnh hưởng đến trạng thái cân bằng lực hút-tĩnh điện. Khi điều này xảy ra, người ta nói rằng có sự chuyển pha và do đó chất rắn thể hiện các tính chất vật lý mới (như ánh và màu).
Ag2S ở nhiệt độ bình thường (thấp hơn 179ºC), nó có cấu trúc tinh thể đơn hình (α- Ag2S). Bên cạnh pha rắn này còn có hai pha khác: bcc (khối trung tâm trong cơ thể) trong khoảng 179 đến 586ºC và fcc (khối trung tâm ở mặt) ở nhiệt độ rất cao (-Ag2S).
Khoáng vật argentit bao gồm pha fcc, còn được gọi là-Ag2S. Một khi được làm mát và biến thành một vách đá, các đặc điểm cấu trúc của chúng chiếm ưu thế kết hợp. Do đó, cả hai cấu trúc tinh thể cùng tồn tại: monoclinic và bcc. Do đó, chất rắn màu đen với âm bội sáng và thú vị xuất hiện.
Thuộc tính
Trọng lượng phân tử
247,80 g / mol
Ngoại hình
Tinh thể màu đen xám
Mùi
Nhà vệ sinh.
Điểm nóng chảy
836 CC. Giá trị này đồng ý với thực tế là Ag2S là một hợp chất có ít tính chất ion và do đó, tan chảy ở nhiệt độ dưới 1000ºC.
Độ hòa tan
Trong nước chỉ 6,21 10-15 g / L ở 25 CC. Đó là, lượng chất rắn màu đen được hòa tan là không đáng kể. Điều này, một lần nữa, là do đặc tính cực nhỏ của liên kết Ag - S, nơi không có sự khác biệt đáng kể về độ âm điện giữa cả hai nguyên tử.
Ngoài ra, Ag2S không tan trong tất cả các dung môi. Không có phân tử nào có thể phân tách hiệu quả các lớp tinh thể của nó trong các ion Ag+ và S2- giải thể.
Cấu trúc
Bốn lớp liên kết S - Ag - S cũng có thể được nhìn thấy trong hình ảnh của cấu trúc, chúng di chuyển lên nhau khi vật rắn được hiểu. Hành vi này có nghĩa là, mặc dù là chất bán dẫn, nó dễ uốn như nhiều kim loại ở nhiệt độ phòng.
Các lớp S-Ag-S phù hợp chính xác vì hình học góc cạnh của chúng được quan sát như một hình zigzag. Có một lực hiểu biết, chúng di chuyển trên một trục dịch chuyển, do đó gây ra các tương tác không cộng hóa trị mới giữa các nguyên tử bạc và lưu huỳnh.
Chỉ số khúc xạ
2.2
Hằng số điện môi
6
Điện tử
Ag2S là một chất bán dẫn lưỡng tính, nghĩa là nó hoạt động như thể nó thuộc loại n và thuộc loại p. Nó cũng không dễ vỡ, vì vậy nó đã được nghiên cứu cho ứng dụng của nó trong các thiết bị điện tử.
Phản ứng khử
Ag2S có thể được khử thành bạc kim loại bằng cách tắm các mảnh màu đen bằng nước nóng, NaOH, nhôm và muối. Phản ứng sau đây diễn ra:
3g2S (s) + 2Al (s) + 3H2O (l) => 6Ag (s) + 3H2S (ac) + Al2Ôi3(s)
Danh pháp
Bạc, có cấu hình điện tử là [Kr] 4d105 giây1, nó chỉ có thể mất một điện tử: đó là 5 quỹ đạo ngoài cùng của nó. Do đó, cation Ag+ Vẫn với cấu hình điện tử [Kr] 4d10. Do đó, nó có hóa trị duy nhất là +1, xác định cách gọi các hợp chất của nó.
Mặt khác, lưu huỳnh có cấu hình điện tử [Ne] 3s23p4, và nó cần hai electron để hoàn thành octet hóa trị của nó. Khi thu được hai electron này (từ bạc), nó biến đổi thành anion lưu huỳnh, S2-, với cấu hình [Ar]. Đó là, isoelectronic đối với khí quý tộc argon.
Vậy là Ag2S phải được gọi theo danh pháp sau:
Hệ thống
Khỉlưu huỳnh dibạc Ở đây chúng tôi xem xét số lượng nguyên tử của mỗi nguyên tố và được biểu thị bằng các tiền tố của tử số Hy Lạp.
Chứng khoán
Bạc sunfua. Khi có hóa trị duy nhất là +1, nó không được chỉ định bằng chữ số La Mã trong ngoặc đơn: bạc sunfua (I); cái nào không đúng.
Truyền thống
Sulfuro argéntico. Vì bạc "hoạt động" với hóa trị +1, hậu tố -ico được thêm vào tên của nó argentum trong tiếng Latin.
Công dụng
Một số cách sử dụng mới cho Ag2S là những người sau đây:
-Các màu dung dịch của hạt nano của chúng (với các kích cỡ khác nhau), có hoạt tính kháng khuẩn, không độc hại, và do đó có thể được sử dụng trong các lĩnh vực y học và sinh học.
-Các hạt nano của chúng có thể tạo thành cái gọi là chấm lượng tử. Chúng hấp thụ và phát ra bức xạ với cường độ lớn hơn nhiều phân tử huỳnh quang hữu cơ, vì vậy chúng có thể thay thế cái sau như là các dấu hiệu sinh học.
-Các cấu trúc của α-Ag2S làm cho nó thể hiện các thuộc tính điện tử nổi bật được sử dụng làm pin mặt trời. Nó cũng đại diện cho một điểm khởi đầu để tổng hợp các vật liệu và cảm biến nhiệt điện mới.
Tài liệu tham khảo
- Đánh dấu Peplow. (Ngày 17 tháng 4 năm 2018). Chất bán dẫn bạc sunfua trải dài như kim loại. Lấy từ: cen.acs.org
- Hợp tác: Tác giả và biên tập viên của cấu trúc tinh thể tập III / 17E-17F-41C () Bạc sunfua (Ag2S). Trong: Madelung O., Rössler U., Schulz M.. Springer, Berlin, Heidelberg.
- Wikipedia. (2018). Bạc sunfua. Lấy từ: en.wikipedia.org
- Stanislav I. Sadovnikov & col. (Tháng 7/2016). Ag2Các hạt nano bạc sunfua và dung dịch keo: Tổng hợp và tính chất. Lấy từ: scTHERirect.com
- Vật liệu Azo. (2018). Bạc sunfua (Ag2S) Chất bán dẫn. Lấy từ: azom.com
- A. Nwofe. (2015). Triển vọng và thách thức của màng mỏng bạc sunfua: Một đánh giá. Phòng Khoa học Vật liệu & Năng lượng tái tạo, Khoa Vật lý Công nghiệp, Đại học bang Ebonyi, Abakaliki, Nigeria.
- UMassAmherst. (2011). Thuyết minh bài giảng: làm sạch bạc xỉn màu. Lấy từ: speechuredemos.chem.umass.edu
- Học tập. (2018). Bạc sunfua là gì? - Công thức hóa học & Công dụng. Lấy từ: học.com


