Hiệu suất xúc tác sinh học và ví dụ
Một chất xúc tác sinh học o chất sinh học là một phân tử, thường có nguồn gốc protein, có khả năng tăng tốc các phản ứng hóa học xảy ra bên trong cơ thể sống. Các phân tử protein xúc tác là các enzyme và những chất có bản chất RNA là ribozyme. Trong bài viết này, chúng tôi sẽ tập trung vào khám phá các enzyme, là chất xúc tác sinh học được biết đến nhiều nhất.
Trong trường hợp không có enzyme, số lượng lớn các phản ứng diễn ra trong tế bào và cho phép sự sống, không thể xảy ra. Chúng có trách nhiệm đẩy nhanh quá trình theo thứ tự cường độ gần 106 - và trong một số trường hợp lớn hơn nhiều.
Chỉ số
- 1 Xúc tác
- 2 enzyme
- 2.1 Enzim là gì?
- 2.2 Đặc điểm của enzyme
- 2.3 Danh pháp và phân loại enzyme
- 2.4 Enzim hoạt động như thế nào?
- 2.5 Thuốc ức chế men
- 2.6 ví dụ
- 3 Sự khác biệt giữa chất xúc tác sinh học (enzyme) và chất xúc tác hóa học
- 3.1 Phản ứng được xúc tác bởi enzyme xảy ra nhanh hơn
- 3.2 Hầu hết các enzyme hoạt động ở điều kiện sinh lý
- 3.3 Tính đặc hiệu
- 3.4 Quy định enzyme là chính xác
- 4 tài liệu tham khảo
Xúc tác
Chất xúc tác là một phân tử có khả năng thay đổi tốc độ của phản ứng hóa học mà không bị tiêu hao trong phản ứng nói trên.
Phản ứng hóa học liên quan đến năng lượng: các phân tử ban đầu liên quan đến phản ứng hoặc chất phản ứng bắt đầu với một mức độ năng lượng. Một lượng năng lượng bổ sung được hấp thụ để đạt đến "trạng thái chuyển tiếp". Sau đó, năng lượng được giải phóng với các sản phẩm.
Sự khác biệt năng lượng giữa các chất phản ứng và các sản phẩm được biểu thị bằng ΔG. Nếu mức năng lượng của các sản phẩm lớn hơn các chất phản ứng, thì phản ứng là nội sinh và không tự phát. Ngược lại, nếu năng lượng của các sản phẩm thấp hơn, phản ứng là ngoại sinh và tự phát.
Tuy nhiên, nếu một phản ứng là tự phát, điều đó không có nghĩa là nó sẽ xảy ra với tốc độ đáng kể. Tốc độ của phản ứng phụ thuộc vào ΔG * (dấu hoa thị đề cập đến năng lượng kích hoạt).
Người đọc phải ghi nhớ các khái niệm này để hiểu cách thức hoạt động của các enzyme xảy ra.
Enzyme
Enzim là gì?
Enzyme là các phân tử sinh học có độ phức tạp đáng kinh ngạc, bao gồm chủ yếu là protein. Protein, lần lượt, là chuỗi axit amin dài.
Một trong những đặc điểm nổi bật nhất của enzyme là tính đặc hiệu của chúng trong phân tử đích - phân tử này được gọi là cơ chất.
Đặc điểm của enzyme
Enzyme tồn tại dưới nhiều hình thức. Một số được cấu tạo hoàn toàn từ protein, trong khi một số khác có các vùng phi protein gọi là cofactors (kim loại, ion, phân tử hữu cơ, v.v.).
Do đó, apoenzyme là một enzyme không có đồng yếu tố của nó và sự kết hợp giữa apoenzyme và đồng yếu tố của nó được gọi là holoenzyme.
Chúng là các phân tử có kích thước lớn đáng kể. Tuy nhiên, chỉ có một vị trí nhỏ của enzyme tham gia trực tiếp vào phản ứng với cơ chất và vùng này là vị trí hoạt động.
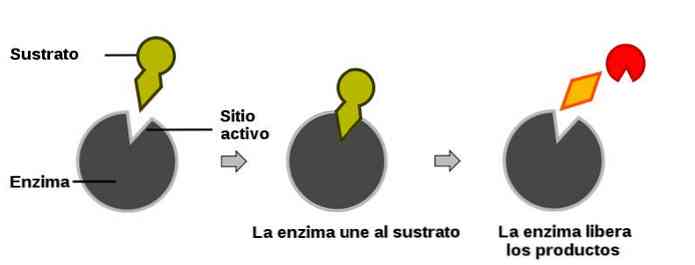
Khi phản ứng bắt đầu, enzyme được ghép với cơ chất của nó như là một khóa được ghép với khóa của nó (mô hình này là sự đơn giản hóa quá trình sinh học thực tế, nhưng phục vụ để minh họa quá trình).
Tất cả các phản ứng hóa học xảy ra trong cơ thể chúng ta đều được xúc tác bởi các enzyme. Trên thực tế, nếu các phân tử này không tồn tại, chúng ta sẽ phải chờ hàng trăm hoặc hàng ngàn năm để các phản ứng hoàn tất. Do đó, quy định về hoạt động của enzyme phải được kiểm soát một cách rất cụ thể.
Danh pháp và phân loại enzyme
Khi chúng ta thấy một phân tử có tên kết thúc bằng -ase, chúng ta có thể chắc chắn rằng đó là một enzyme (mặc dù có những ngoại lệ cho quy tắc này, chẳng hạn như trypsin). Đây là quy ước để chỉ định tên của các enzyme.
Có sáu loại enzyme cơ bản: oxyoreductase, transferase, hydrolase, lyase, isomeraes và ligase; chịu trách nhiệm: phản ứng oxi hóa khử, chuyển nguyên tử, thủy phân, bổ sung liên kết đôi, đồng phân hóa và liên kết của các phân tử, tương ứng.
Enzim hoạt động như thế nào?
Trong phần xúc tác, chúng tôi đã đề cập rằng tốc độ của phản ứng phụ thuộc vào giá trị của G *. Giá trị này càng cao, phản ứng càng chậm và chậm. Enzim chịu trách nhiệm giảm tham số đã nói - do đó làm tăng tốc độ phản ứng.
Sự khác biệt giữa các sản phẩm và các chất phản ứng vẫn giống hệt nhau (enzyme không ảnh hưởng đến nó), cũng như sự phân phối của cùng một. Enzim tạo điều kiện cho sự hình thành trạng thái chuyển tiếp.
Ức chế enzyme
Trong bối cảnh nghiên cứu về enzyme, chất ức chế là những chất có khả năng làm giảm hoạt động của chất xúc tác. Chúng được phân thành hai loại: chất ức chế cạnh tranh và không cạnh tranh. Những loại đầu tiên cạnh tranh với chất nền và những loại khác thì không.
Nói chung, quá trình ức chế là có thể đảo ngược, mặc dù một số chất ức chế có thể vẫn được kết hợp với enzyme gần như vĩnh viễn.
Ví dụ
Có một lượng lớn enzyme trong các tế bào của chúng ta - và trong các tế bào của tất cả các sinh vật sống. Tuy nhiên, nổi tiếng nhất là những người tham gia vào quá trình trao đổi chất như glycolysis, chu trình Krebs, chuỗi vận chuyển điện tử, trong số những người khác..
Succinate dehydrogenase là một loại enzyme oxyoreductase xúc tác quá trình oxy hóa succinate. Trong trường hợp này, phản ứng liên quan đến việc mất hai nguyên tử hydro.
Sự khác biệt giữa chất xúc tác sinh học (enzyme) và chất xúc tác hóa học
Có những chất xúc tác có bản chất hóa học, giống như chất sinh học, làm tăng tốc độ phản ứng. Tuy nhiên, có sự khác biệt đáng chú ý giữa cả hai loại phân tử.
Phản ứng xúc tác enzyme xảy ra nhanh hơn
Đầu tiên, các enzyme quản lý để tăng tốc độ của các phản ứng theo thứ tự cường độ gần bằng 106 lên đến 1012. Chất xúc tác hóa học cũng tăng tốc độ, nhưng chỉ một vài bậc độ lớn.
Hầu hết các enzyme hoạt động ở điều kiện sinh lý
Khi các phản ứng sinh học được thực hiện bên trong cơ thể sống, điều kiện tối ưu của chúng bao quanh các giá trị sinh lý của nhiệt độ và pH. Mặt khác, các nhà hóa học cần các điều kiện quyết liệt về nhiệt độ, áp suất và độ axit.
Tính đặc hiệu
Enzyme rất cụ thể trong các phản ứng mà chúng xúc tác. Trong hầu hết các trường hợp, chúng chỉ hoạt động với một chất nền hoặc với một số ít. Tính đặc hiệu cũng áp dụng cho loại sản phẩm họ sản xuất. Phạm vi cơ chất của các chất xúc tác hóa học rộng hơn nhiều.
Các lực xác định tính đặc hiệu của sự tương tác giữa enzyme và cơ chất của nó là giống nhau quyết định cấu tạo của cùng một protein (tương tác Van der Waals, tĩnh điện, liên kết hydro và kỵ nước).
Các quy định enzyme là chính xác
Cuối cùng, các enzyme có khả năng điều tiết lớn hơn và hoạt động của các chất này thay đổi tùy theo nồng độ của các chất khác nhau trong tế bào.
Trong số các cơ chế điều hòa, chúng tôi tìm thấy sự kiểm soát allosteric, sự biến đổi cộng hóa trị của các enzyme và sự thay đổi số lượng enzyme được tổng hợp.
Tài liệu tham khảo
- Berg, J. M., Stasher, L., & Tymoczko, J. L. (2007). Hóa sinh. Tôi đã đảo ngược.
- Campbell, M. K., & Farrell, S. O. (2011). Hóa sinh Phiên bản thứ sáu. Thomson. Brooks / Cole.
- Devlin, T. M. (2011). Sách giáo khoa hóa sinh. John Wiley & Sons.
- Koolman, J., & Röhm, K. H. (2005). Hóa sinh: văn bản và tập bản đồ. Ed. Panamericana Y tế.
- Mougios, V. (2006). Bài tập hóa sinh. Động học của con người.
- Müller-Esterl, W. (2008). Hóa sinh Nguyên tắc cơ bản cho y học và khoa học đời sống. Tôi đã đảo ngược.
- Poortmans, J.R. (2004). Nguyên tắc hóa sinh. Karger.
- Voet, D., & Voet, J. G. (2006). Hóa sinh. Ed. Panamericana Y tế.


