Nền tảng nhuộm Gram, vật liệu, kỹ thuật và sử dụng
các Nhuộm gram là kỹ thuật nhuộm đơn giản và hữu ích nhất trong vi sinh chẩn đoán. Kỹ thuật này được tạo ra bởi bác sĩ người Đan Mạch Hans Christian Gram vào năm 1884, người đã tìm cách phân loại vi khuẩn theo Gram dương và Gram âm, theo thành phần của thành tế bào.
Kỹ thuật này đã trải qua một số sửa đổi của Hucker vào năm 1921 để ổn định thuốc thử và cải thiện chất lượng của vết bẩn, do đó vết Gram còn được gọi là Gram-Hucker.
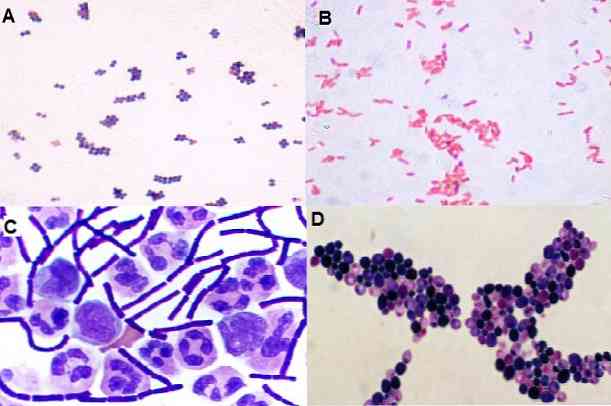
Với kỹ thuật này, người ta cũng có thể quan sát hình thức mà các vi sinh vật có, đó là liệu chúng có phải là cocci, trực khuẩn, coccobacilli, pleomorphic, dạng sợi, trong số những loại khác. Cũng như sự phân bố của nó trong không gian: theo cụm, theo chuỗi, bị cô lập, theo cặp, theo hình tứ giác, v.v..
Khi nghi ngờ nhiễm vi khuẩn, hầu hết các mẫu nhận được phải được trải trên một phiến kính và nhuộm Gram để kiểm tra dưới kính hiển vi..
Báo cáo của Gram sẽ hướng dẫn bác sĩ về loại vi sinh vật nào có thể là nguyên nhân gây nhiễm trùng, trước khi có được kết quả cuối cùng của vụ mùa.
Trong một số trường hợp, cuộc sống của bệnh nhân rất bị tổn hại, vì vậy các bác sĩ rất cần báo cáo Gram để điều trị theo kinh nghiệm, trong khi chờ xác định vi sinh vật..
Ví dụ, nếu Gram tiết lộ rằng có cầu khuẩn Gram dương trong dịch não tủy, bác sĩ sẽ định hướng điều trị ban đầu bằng kháng sinh loại trừ loại vi khuẩn này, theo các giao thức được thiết lập cho nó..
Một khi kết quả cuối cùng đến với tên của vi sinh vật bị cô lập và kháng sinh tương ứng, bác sĩ sẽ đánh giá xem có nên thay đổi trị liệu hay không. Quyết định này sẽ được đưa ra theo nghiên cứu về tính nhạy cảm của vi sinh vật đối với các loại kháng sinh mà nó đang nhận và sự tiến hóa của bệnh nhân.
Chỉ số
- 1 nền tảng
- 2 Vật liệu
- 3 Chuẩn bị thuốc nhuộm và thuốc thử
- 3.1 Dung dịch tím pha lê
- 3.2 Iodo-Lugol
- 3.3 Tẩy trắng
- 3,4 Tương phản
- 4 Bảo quản thuốc thử
- 5 Chuẩn bị sự lan truyền của mẫu được tô màu
- 5.1 -Gram mẫu trực tiếp
- 5.2 -Gram của cây trồng
- 6 Kỹ thuật
- 7 Tiện ích
- 8 lỗi thường gặp
- 9 Tài liệu tham khảo
Nền tảng
Đây là một kỹ thuật trình bày 4 bước cơ bản: nhuộm màu, cố định với sự phù hợp, đổi màu và tương phản. Do đó, kỹ thuật này ngoài việc tạo màu cho vi khuẩn, còn phân biệt chúng.
Pha lê tím là chất màu đầu tiên được sử dụng. Nó có ái lực với peptidoglycan và màu tím sẽ nhuộm tất cả các vi khuẩn có mặt, sau đó lugol được đặt, hoạt động như một chất gắn màu, nghĩa là, nó sẽ tạo ra sự hình thành các phức hợp không hòa tan của protein tím-iốt - tinh thể trong tế bào.
Vi khuẩn gram dương, có thành dày peptidoglycan, tạo thành phức chất hơn (tinh thể tím-iốt), do đó chúng giữ lại thuốc nhuộm.
Nó cũng ảnh hưởng đến thành vi khuẩn gram dương chứa một lượng lớn axit không bão hòa hơn, cho thấy ái lực cao đối với các tác nhân oxy hóa (Lugol).
Trong khi đó, vi khuẩn gram âm có một lớp peptidoglycan mỏng, khiến vi khuẩn ít phức tạp hơn vi khuẩn gram dương.
Sau đó là bước đổi màu, trong đó vi khuẩn Gram dương và Gram âm hoạt động khác nhau.
Vi khuẩn gram âm chứa một màng ngoài giàu lipopolysacarit là một phần của thành tế bào của nó. Chất béo bị phá hủy do tiếp xúc với rượu acetone, do đó màng ngoài bị mất ổn định, tinh thể màu tím được giải phóng.
Đây là cách nó được thay thế bằng safranin hoặc fuchsin cơ bản, lấy màu đỏ.
Trong trường hợp vi khuẩn gram dương, chúng chống lại sự đổi màu vì chất tẩy có tác dụng se khít lỗ chân lông, ngăn không cho phức hợp tinh thể tím / iốt thoát ra.
Do đó, màu sắc với tinh thể màu tím là ổn định, và không có chỗ cho safranin hoặc fuchsin. Bởi vì điều này, những vi khuẩn nhuộm màu xanh hoặc tím dữ dội.
Vật liệu
Bộ màu Gram bao gồm:
- Pha lê tím
- Lugol
- Rượu axetone
- Safranin hoặc fuchsin cơ bản
Chuẩn bị thuốc nhuộm và thuốc thử
Dung dịch pha lê tím
Giải pháp A:
Pha lê tím -2 gr
Rượu etylic 95% -20cc
Giải pháp B:
Amoni oxalat -0,8 gr
Nước cất-80 cc
Để chuẩn bị cuối cùng cho tinh thể tím, dung dịch 1:10 nên được pha loãng với nước cất và trộn với 4 phần dung dịch B. Hỗn hợp được bảo quản trong 24 giờ trước khi sử dụng. Nó được lọc trong bình để nhuộm màu hổ phách bằng bộ lọc giấy.
Số lượng sẽ được sử dụng hàng ngày được chuyển vào một chai màu hổ phách với ống nhỏ giọt.
Iodo-Lugol
Cân và đo lượng chỉ định của từng hợp chất, như sau:
Tinh thể của Iodo --1gr
Kali Iodide - 2gr
Nước cất -300 cc
Kali iodide hòa tan từng chút một trong nước và sau đó bổ sung iốt. Dung dịch được cạo thành chai màu hổ phách.
Số lượng sẽ được sử dụng hàng ngày được chuyển vào một chai hổ phách nhỏ hơn với ống nhỏ giọt.
Tẩy trắng
Rượu ethyl 95% -50 ml
Acetone - 50 ml
Nó được chuẩn bị trong các phần bằng nhau. Che phủ tốt, nó có xu hướng bay hơi.
Đặt trong một chai với ống nhỏ giọt.
Chuẩn bị này cung cấp một sự đổi màu trong thời gian vừa phải 5-10 giây và được khuyến nghị nhất.
Người mới bắt đầu chỉ thích sử dụng cồn ethyl 95%, trong đó sự đổi màu chậm hơn từ 10 đến 30 giây.
Mặc dù người có kinh nghiệm nhất có thể sử dụng acetone tinh khiết, trong đó sự đổi màu xảy ra rất nhanh từ 1 đến 5 giây.
Tương phản
Giải pháp chứng khoán Safranin
Safranina -2,5 gr
Rượu etylic 95% -100 cc
Sau khi cân, lượng safranin được chỉ định hòa tan trong 100 cc rượu ethyl đến 95%.
Các giải pháp safranin làm việc được chuẩn bị từ các giải pháp chứng khoán.
Để làm điều này, đo 10 cc dung dịch gốc, thêm 90 cc nước cất để hoàn thành 100 ml.
Nên chuyển số tiền sẽ được sử dụng hàng ngày vào chai màu hổ phách bằng ống nhỏ giọt.
Các vi sinh vật nhuộm Gram âm yếu với vết Gram-Hucker, chẳng hạn như vi khuẩn kỵ khí nhất định, Legionella sp, Campylobacter sp và Brucella sp, chúng có thể được nhuộm màu tốt hơn nhiều nếu việc sửa đổi được tạo bởi Kopeloff thành nhuộm Gram-Hucker, được gọi là nhuộm Gram-Kopeloff, được sử dụng.
Kỹ thuật này thay đổi thuốc nhuộm safranin bằng fuchsin cơ bản. Với sửa đổi này, có thể tô màu hiệu quả các vi sinh vật đã nói ở trên.
Bảo quản thuốc thử
Thuốc nhuộm đã pha chế nên được bảo quản ở nhiệt độ phòng.
Chuẩn bị mẫu trải ra màu
Một mẫu phải chứa ít nhất 105 vi sinh vật trước khi quan sát vi sinh vật trong một vết bẩn có khả năng. Lây lan có thể được thực hiện từ mẫu trực tiếp hoặc nuôi cấy trong môi trường rắn hoặc lỏng.
Các chênh lệch phải đồng đều, phân bố tốt và không quá dày, để hình dung rõ hơn về các cấu trúc hiện tại.
-Gram mẫu trực tiếp
Gram nước tiểu không cần ly tâm
Nước tiểu được trộn và 10 μl được đặt trên một slide. Việc quan sát ít nhất một vi khuẩn / Trường ngâm cho thấy có nhiễm trùng.
Điều này có nghĩa là văn hóa sẽ có khoảng hơn 100.000 CFU / ml (105 CFU / mL) nước tiểu trong 85% trường hợp.
Phương pháp này không hữu ích cho số lượng thuộc địa dưới 100.000 CFU.
Gram LCR
CSF nên được ly tâm, loại bỏ phần nổi phía trên và viên trải trên một slide. Chất lỏng này được vô trùng trong điều kiện bình thường; sự quan sát của vi khuẩn cho thấy nhiễm trùng.
Gram mẫu hô hấp
Dịch rửa đờm Gram, phế quản hoặc phế quản, mặc dù có thể có nhiều loại vi sinh vật, sẽ luôn luôn hướng dẫn trong chẩn đoán, bên cạnh việc hữu ích là loại tế bào được quan sát.
Trong trường hợp đờm, phết tế bào phải được chuẩn bị với các phần có độ tinh khiết nhất của mẫu.
Phân Gram
Không nên thực hiện Gram cho loại mẫu này, vì nó không có giá trị chẩn đoán.
-Cây trồng gram
Chúng có thể được thực hiện theo hai cách, một từ cây trồng lỏng và cách khác từ cây trồng rắn.
Cây trồng lỏng
Từ nuôi cấy lỏng, nó cực kỳ đơn giản; dưới cái bật lửa, vài vòng quay của nước dùng đục được lấy và chúng được đặt trên một phiến khô và sạch, tạo ra các chuyển động tròn từ tâm về phía ngoại vi, để phân phối vật liệu đồng đều.
Nó được phép để khô tự nhiên trong không khí. Sau khi khô, vật liệu được cố định vào tấm bằng nhiệt. Đối với điều này, với sự trợ giúp của kẹp, tờ 3 được truyền 4 lần qua ngọn lửa của đầu đốt Bunsen, chú ý không làm cháy vật liệu.
Tấm được làm mát và đặt trên cầu màu.
Cây trồng rắn
Để thực hiện mở rộng cho nhuộm Gram từ một nền văn hóa vững chắc, hãy tiến hành như sau:
Trước khi chọn các khuẩn lạc được lấy, nên chuẩn bị slide, đặt hai giọt dung dịch muối sinh lý vô trùng.
Nếu đĩa nuôi cấy ban đầu chứa một số loại khuẩn lạc khác nhau, một thuộc địa riêng biệt của từng loài sẽ được chọn để thực hiện Gram. Mỗi thuộc địa sẽ được lấy bằng vòng bạch kim để hòa tan nó trong dung dịch muối được đặt trước đó trên phiến kính.
Chuyển động tròn được đưa ra từ trung tâm đến ngoại vi, để phân phối thuộc địa đồng nhất trên slide..
Nó được phép để khô tự nhiên trong không khí. Sau khi làm khô tấm được cố định bằng nhiệt, như đã giải thích ở trên (đốt lửa bằng nắp bật lửa), cẩn thận không làm cháy vật liệu.
Thủ tục này phải được thực hiện với từng loại thuộc địa khác nhau. Trên một tờ giấy, thứ tự quan sát cần được lưu ý, ví dụ:
Thuộc địa 1: Thuộc địa tan máu beta vàng: cầu trùng gram dương được quan sát thấy trong các cụm
Thuộc địa 2: Thuộc địa kem, không tan máu: Coccobacilli gram âm đã được quan sát.
Mỗi tờ phải được dán nhãn để biết những gì chúng ta đang quan sát.
Kỹ thuật
Kỹ thuật nhuộm gram cực kỳ đơn giản để thực hiện và tương đối rẻ tiền và không thể bỏ qua trong phòng thí nghiệm vi sinh.
Điều tương tự được thực hiện như sau:
- Khắc phục vết bẩn bằng nhiệt và đặt lên cây cầu màu.
- Tấm được phủ hoàn toàn bằng kính màu tím trong 1 phút.
- Rửa bằng nước. Không khô
- Đậy đĩa bằng dung dịch Lugol, để trong 1 phút. Rửa bằng nước. Không khô.
- Discolor 5-10 giây với rượu khuấy acetone nhẹ nhàng. O định vị tấm thẳng đứng và decolorizing giọt rơi trên bề mặt cho đến khi kéo dư thừa tinh thể tím unretained. không vượt quá.
- Rửa bằng nước. Không khô.
- Thay thế các tấm vào màu sắc cầu và bao gồm 30 giây với safranin (Gram Hucker) hoặc 1 phút với fuchsin cơ bản (Gram Kopeloff).
- Rửa bằng nước
- Để khô tự nhiên trong không khí thẳng đứng.
Sau khi khô, đặt 1 giọt dầu ngâm để quan sát nó dưới vật kính 100X trong kính hiển vi quang học.
Tiện ích
Kỹ thuật này cho phép phân biệt sự khác biệt về hình thái của hầu hết các vi khuẩn.
Nấm men cũng được phân biệt bởi màu này. Họ lấy màu tím pha lê, nghĩa là họ nhuộm Gram dương.
Hơn nữa, người ta có thể phân biệt Gram dương bào tử hình thành, trong đó một không gian rõ ràng trong phạm vi trực khuẩn nơi endospore hình thành, mặc dù các bào tử không gây bẩn chấp hành tốt. các kỹ thuật khác cho bào tử nhuộm màu được sử dụng như Shaeffer-Fulton.
Cần lưu ý rằng vết này không phục vụ cho màu tất cả các loại vi khuẩn, đó là, có những trường hợp vết bẩn không hoạt động.
Trong trường hợp này, vi khuẩn thiếu thành tế bào có thể được đề cập. Ví dụ: chi Mycoplasma, spheroplasts, Ureaplasma, L-form và protoplasts.
Nó cũng nhuộm màu vi khuẩn xấu với các bức tường giàu axit mycolic, chẳng hạn như Mycobacteria và vi khuẩn nội bào như Chlamydias và Rickettsias.
Nó cũng không hiệu quả để nhuộm hầu hết các vi khuẩn xoắn khuẩn.
Có những vi khuẩn cùng chi có thể được quan sát trong cùng một mẫu là Gram dương và Gram âm. Khi điều này xảy ra, nó được gọi là nhuộm Gram biến đổi, có thể là do sự thay đổi trong chất dinh dưỡng, nhiệt độ, pH hoặc nồng độ chất điện giải..
Những lỗi thường gặp
Tẩy trắng quá mức
Phóng đại trong bước đổi màu có thể gây ra sự quan sát của vi sinh vật gram âm giả.
Đừng đợi đủ thời gian sấy để thêm dầu ngâm:
Lỗi này gây ra sự hình thành các mixen béo gây khó khăn cho việc quan sát các cấu trúc hiện tại. Điều này xảy ra khi dầu tham gia vào các phân tử nước có trong vết bẩn.
Đảo ngược thứ tự của thuốc thử:
Một lỗi như thế này sẽ khiến vi khuẩn gram âm hiển thị màu tím, nghĩa là sai Gram dương.
Sử dụng cây trồng cũ (rắn hoặc lỏng):
Nó có thể gây ra vi khuẩn gram dương Gram nhuộm tiêu cực của họ (false Gram âm). Điều này xảy ra bởi vì trong các loại cây trồng cũ có khả năng là vi khuẩn chết hoặc bị hư hỏng và dưới những điều kiện vi khuẩn không giữ lại màu tím tinh thể.
Sử dụng dung dịch Lugol rất cũ:
Cuối cùng, lugol mất tính chất của nó và mất dần màu sắc của nó. Nếu thuốc thử được sử dụng như thoái hóa, điều này sẽ không giải quyết được một trong hai màu tím tinh thể do đó không có khả năng thu được một Gram vi sinh vật tiêu cực hiển thị sai.
Nền màu xanh
Một nền bị đổi màu đúng sẽ có màu đỏ. Một nền màu xanh chỉ ra rằng sự đổi màu là không đủ.
Tài liệu tham khảo
- Ryan KJ, Ray C. 2010. Sherris. Vi sinh Y khoa, phiên bản thứ 6 McGraw-Hill, New York, U.S.A
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Chẩn đoán vi sinh. (Tái bản lần thứ 5). Argentina, Biên tập Panamericana S.A..
- Forbes B, Sahm D, Weissfeld A. 2009. Chẩn đoán vi sinh học của Bailey & Scott. 12 ed. Argentina Panamericana S.A Biên tập
- Casas-Rincón G. 1994. Mycology chung. Ed lần thứ 2 Đại học Trung tâm Venezuela, Phiên bản thư viện. Venezuela, Venezuela.
- "Nhuộm gram" Wikipedia, bách khoa toàn thư miễn phí. Ngày 4 tháng 10 năm 2018, 23:40 UTC. Ngày 9 tháng 12 năm 2018, 17:11. Lấy từ es.wikipedia.org.
- González M, González N. 2011. Hướng dẫn sử dụng vi sinh y học. Tái bản lần 2, Venezuela: Tổng cục truyền thông và ấn phẩm của Đại học Carabobo.
- López-Jácome L, Hernández-Durán M, Colín-Castro C, Ortega-Peña S, Cerón-González G, Franco-Cendejas F. Nhuộm cơ bản trong phòng thí nghiệm vi sinh. Nghiên cứu về người khuyết tật. 2014; 3 (1): 10-18.


